机械力刺激动态多功能人体组织器官模型系统

该系统将3D细胞培养与机械刺激微环境相结合,该系统集成了大多数人体器官生理/疾病状态的关键要素—3D环境和机械刺激,成功研制了下一代跳动片上器官,从而可以提供更可靠,反应迅速且价格合理的临床前模型来筛选药物的益处和安全性。

一、牵张刺激:


能够提供单轴拉伸变形。 它适用于培养体内经历拉伸刺激的所有那些组织(即,心脏,肌腱,肌肉..)。
二、压缩刺激

能够提供压缩刺激。 它适用于培养所有在体内经历压缩刺激的组织(即软骨,骨骼,牙齿等)。
三、多芯片组合模块
可以把4个可牵张或压缩的芯片整合在一起,12个微结构,允许机械刺激每个平台,并以无菌方式光学监控培养物

四、牵张拉伸、压缩刺激仪:
可以定义牵张、压缩、流体剪切的力大小、频率、周期和各种波形。
五、成功创建模型举例:
1、心脏芯片模型,3D心脏组织模型——在体外复制同体内相一致的心脏组织及环境。具有同体内相一致特征心脏组织将大大增加体外实验的准确性
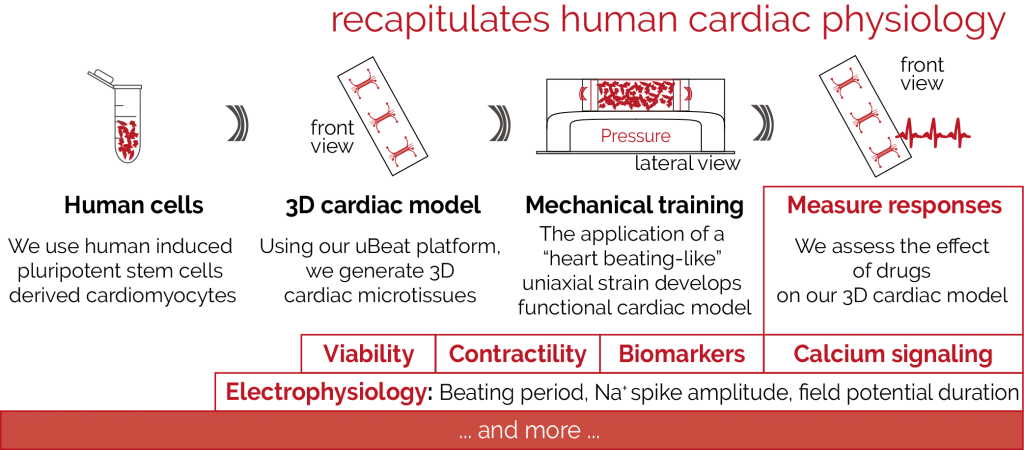
在该系统上开发芯片上功能化的、能跳动的人的心脏的微型模型。 将类似于心脏跳动的机械训练阶段应用于以3D方式培养的人类心脏细胞。 在几天之内,就可以自然并同时跳动生成成熟的人类心脏组织。
可以测量心脏的关键功能,以了解心脏跳动率,结构毒性和电活动的变化。
确实能够像人类心脏一样以剂量依赖性方式对药物做出反应,从而成为筛选药物心脏毒性和抗心律失常药物效率的理想平台。
机械训练诱发整个微组织同步跳动
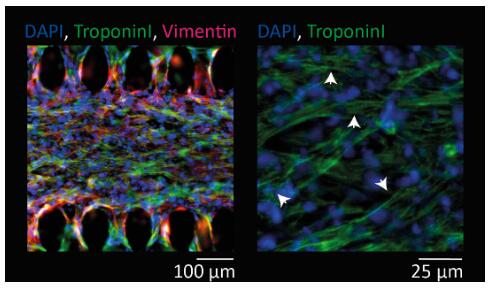
通过在系统芯片中将带有支持性成纤维细胞的心肌细胞培养7天,可得到显示出具有细长形态和典型肌节条纹(心肌肌钙蛋白I染色)的细胞的心脏微组织。
该系统机械训练类似于心脏的生理伸展运动(即10%),其结果对于获得达到前所未有的成熟度和功能水平的心脏组织至关重要

uECG允许在线监测心脏电生理参数
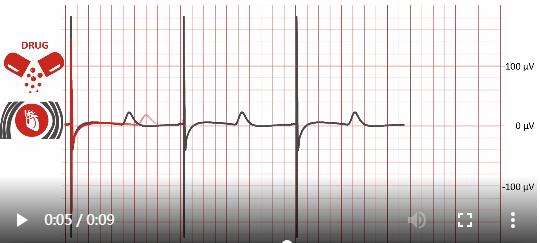
uECG以无创方式在线监测表征培养的心脏微组织的电生理参数。 与uECG集成的该系统牵张提供了一种独特的工具来捕获药物对心脏电的影响
2、体外人类骨关节炎(OA)软骨芯片模型
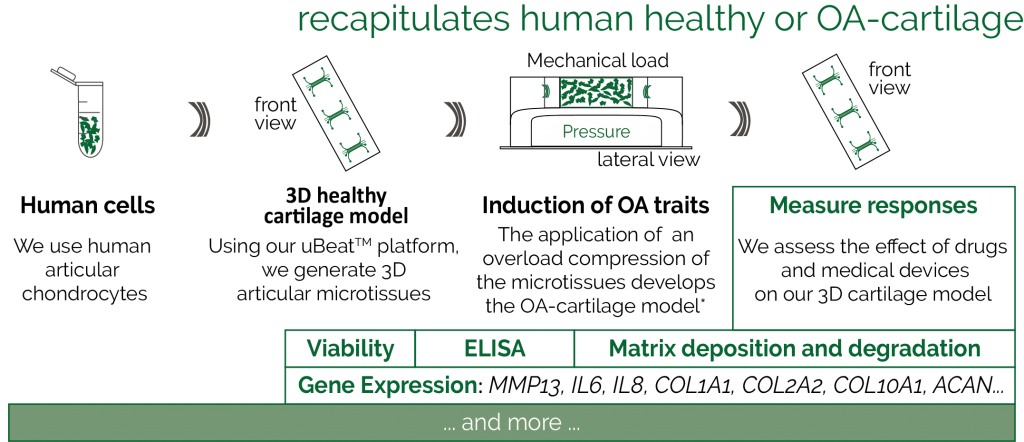
该系统成功开发了业界个体外人类芯片化骨关节炎(OA)软骨微型模型。健康的软骨微结构首先由嵌入水凝胶的人体关节软骨细胞产生,并在系统芯片中静态培养2周。由于采用了我公司机械力调整芯片技术,因此将类似于OA病理条件的机械超负荷应用于健康的软骨微组织。 芯片病理刺激在几天内导致了OA样微组织的产生,其表型和基因型与OA临床证据相关。
该软骨模型提供了OA关键指标的测量,包括合成代谢-代谢平衡变化,炎症的发生,基质降解酶的产生以及关键分子途径的变化。
动物模型和其他体外平台无法在这种程度上模仿人类病理。因此,该软骨模型可用于测试潜在的新型抗OA候选药物逆转病理学的效率,这是个能够复制OA疾病的体外平台。
在系统中生成健康的人类软骨微组织
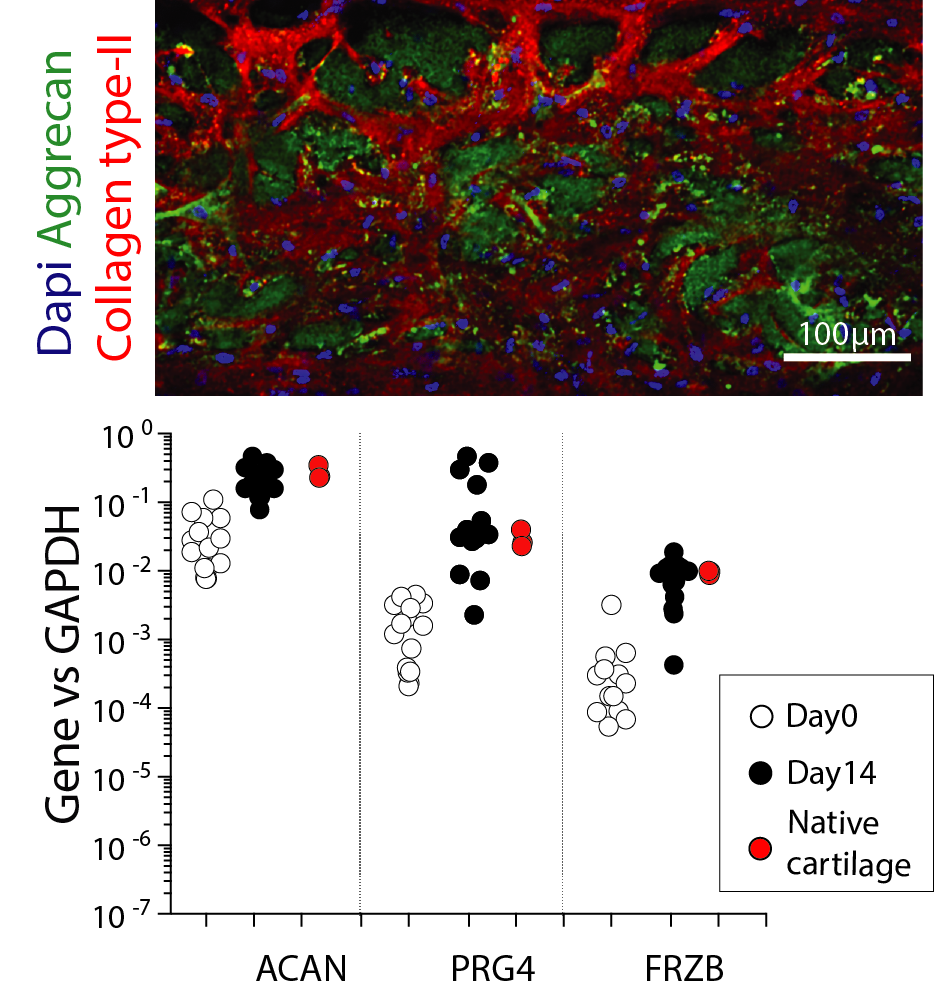
通过在系统中在静态条件下培养人类健康的关节软骨细胞两周,获得了一种软骨微组织,表现出细胞外基质的天然样沉积(II型胶原蛋白和聚集蛋白聚糖含量丰富),并且具有与人类相匹配的特征基因谱软骨。
系统机械过载导致类似OA的合成代谢-分解代谢平衡变化
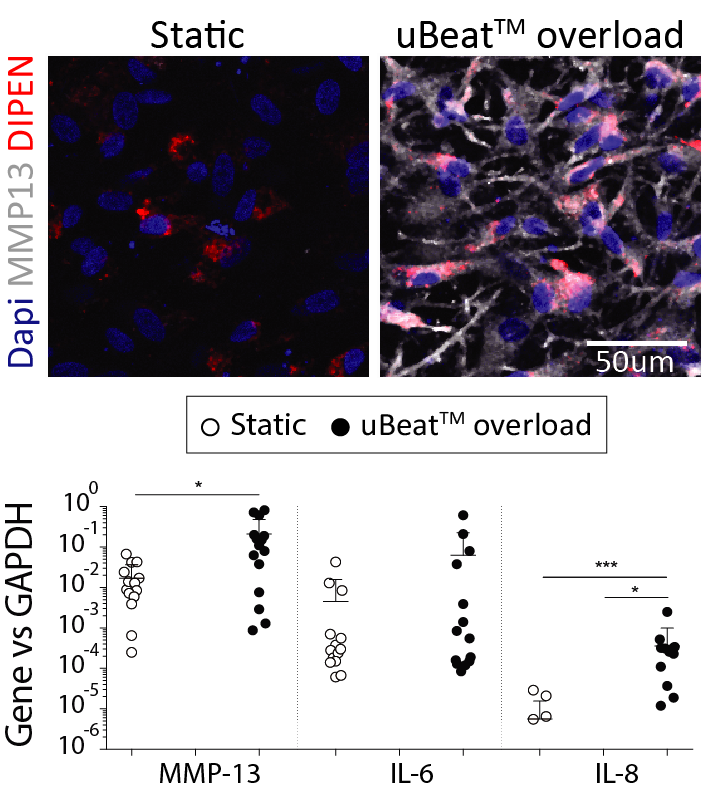
系统病理刺激可引起软骨稳态向分解代谢的转变,这由合成代谢基因(COL2A1和ACAN)的表达缺失,MMP13软骨降解酶的产生增加以及炎症相关基因(IL6和IL8)的上调来证明。
系统诱导出类似OA的基因图谱
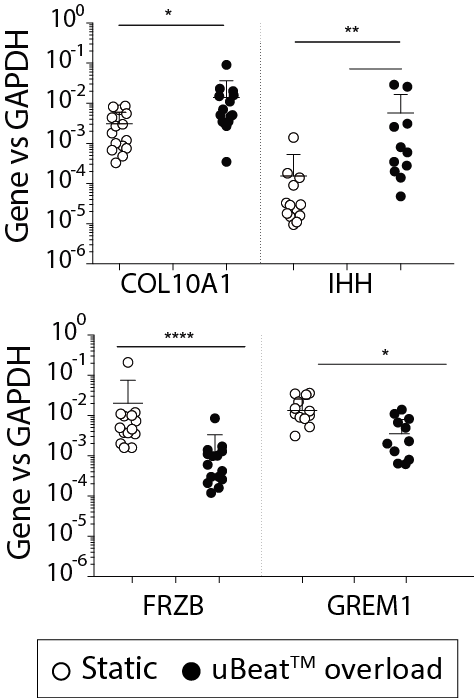
系统病理刺激触发了与OA临床证据兼容的基因表达谱的获取。 COL10A1和IHH表达上调,表明该模型向瞬时钙化软骨的肥大分化触发。 在uBeat?病理刺激下,GREM1,FRZB和DKK1(与OA发病呈负相关的BMP和Wnt信号拮抗剂)下调,其水平与天然OA软骨样品中检测到的水平匹配