此外,铜与肿瘤细胞中的多个信号通路相关,通过结合和激活多个信号通路中的关键分子影响癌症发生 (图 2)。这也加速了用于抗癌治疗的 Cu 配位化合物的开发。
目前已经提出了两种主要策略:1. 使用 Cu 螯合剂来降低 Cu 的生物利用度。2. 使用 Cu 离子载体将 Cu 递送到细胞中以增加细胞内 Cu 水平。
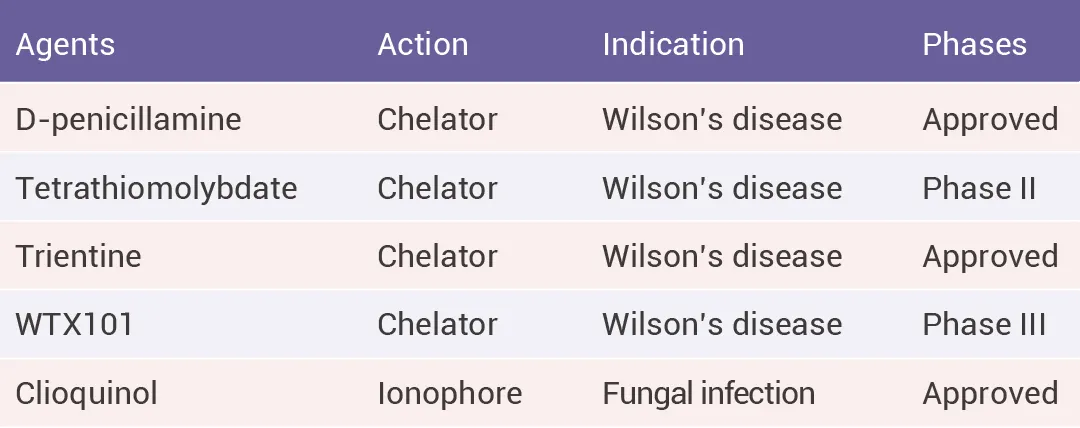
铜离子载体是一种可逆地结合铜离子的脂溶性分子,可诱导铜细胞凋亡。如 Elesclomol 、双(缩氨基硫脲)类似物 [Cu II (atsm)和 Cu II (gtsm)] 以及Disulfiram (DSF) 可提高细胞内 Cu 水平并发挥抗癌活性。其中,DSF 和 ES 受到的关注最多。迄今为止,铜离子载体已进行了多项临床试验 (表 1)。
Elesclomol:可将 Cu 带到线粒体,过量的铜会促进脂化蛋白的聚集和 Fe-S 簇蛋白的不稳定,从而导致蛋白毒性应激并最终导致细胞死亡[7]。Elesclomol 作为候选药物,已被证明可以增强紫杉醇 (Paclitaxel) 在难治性实体瘤患者和 IV 期转移性黑色素瘤患者中的治疗效果。在由晚期黑色素瘤患者组成的 III 期临床试验中,与乳酸脱氢酶 (LDH) 水平高的患者相比,Elesclomol 治疗对 LDH 水平较低的患者 (较低的 LDH 水平代表高线粒体代谢状态) 具有更强的抗肿瘤活性。再次验证了 Elesclomol 对高水平脂酰化 TCA 酶和过度活跃的线粒体呼吸率的细胞更敏感 (详见往期推文:空降"热搜" 铜死亡丨解锁细胞死亡新方式)[3]。 
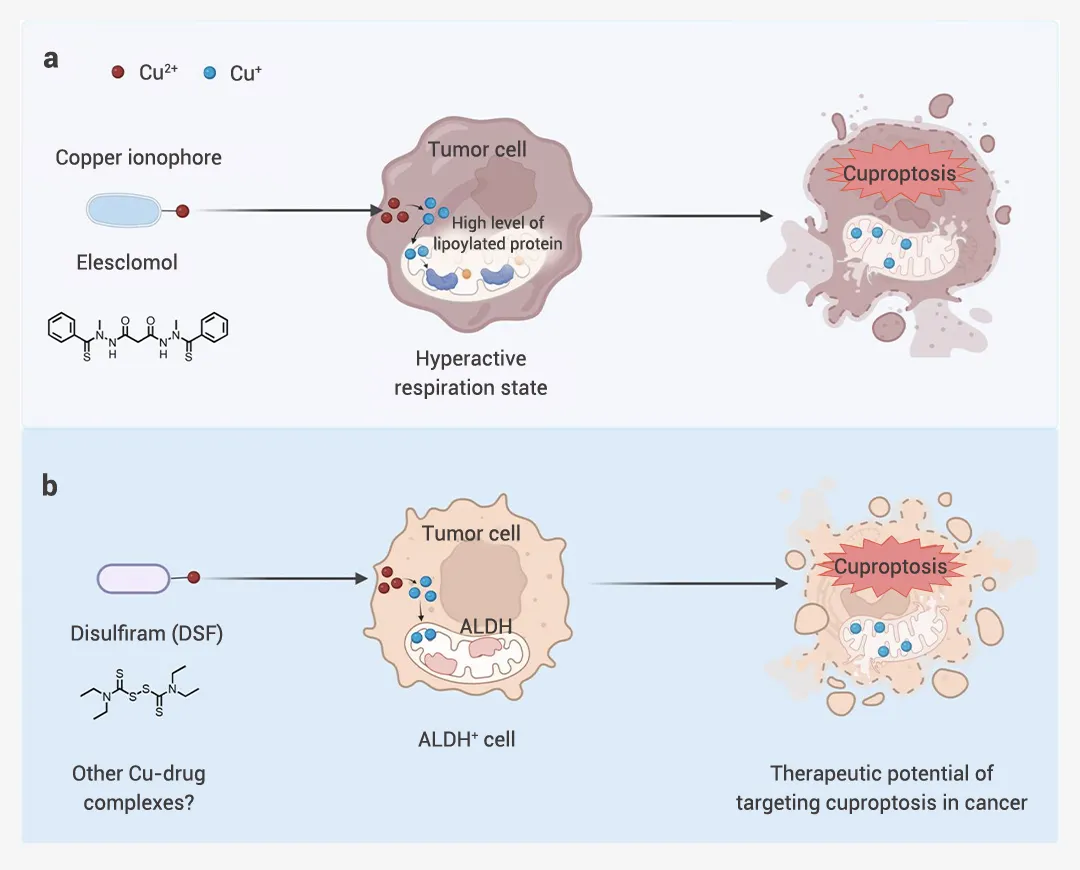
图 3. 针对癌症中铜细胞凋亡的两种潜在治疗策略[4]
a. Cu 离子载体 Elesclomol 被认为会在表达高水平脂化线粒体酶或处于过度活跃呼吸状态的癌细胞中诱导铜凋亡。b. Disulfiram 与 Cu 结合选择性靶向具有高 ALDH 表达的癌细胞。
Disulfiram (DSF):和 Elesclomol 原理一样,DSF 也可以将铜输送到细胞中,诱导铜凋亡。DSF 可以穿过 BBB,在胶质母细胞瘤患者的临床试验中具有抗癌和/或化疗增敏作用。DSF 和 Cu 治疗还可以降低肿瘤抑制基因 PTEN 的表达并激活人类乳腺癌中的 AKT 信号传导。此外,DSF 可抑制醛脱氢酶 (ALDH),选择性靶向并杀死 ALDH+ 癌症干细胞,从而降低肿瘤复发的风险。铜离子载体可与 TKI、PI 等靶向治疗药物联合使用,应用于线粒体代谢状态高的肿瘤[3]。Cu bis (thiosemicarbazone):对于双 (氨基硫脲) 类似物,Cu II (atsm) 在携带结肠癌肿瘤的仓鼠中具有抗癌活性。Cu II (gtsm) 在体外对前列腺癌细胞发挥肿瘤杀伤作用,并显著降低原位小鼠模型中的前列腺癌负担[3]。
除了铜离子载体,使用螯合剂消耗 Cu 已被证明可以通过抑制多种动物模型的病变血管形成来延迟癌症转移。
其中,TTM 的研究最为广泛。使用 TTM 降低 Cu 水平会影响 MEK1/2 激酶的活性和 BRAF 驱动的肿瘤发生,从而减少异种移植的 BRAFV600E 肿瘤的生长。TTM 还可以抑制 Cu 伴侣蛋白,抑制 Cu 向 LOX 等铜酶的输送。此外,在恶性间皮瘤的 II 期试验中发现,TTM 具有抗血管生成作用,可延缓 I 期或 II 期间皮瘤患者的疾病进展[3]。
对于 Trientine,其可以抑制 IL-8 的表达,在肝细胞癌中表现出抗肿瘤作用。Trientine 还可以降低 CD31 表达并抑制内皮细胞增殖。而 D-penicillamine 则可以抑制 LOX 的活性,从而导致胶原蛋白交联形成受损、VEGF 表达减少,延缓体内胶质母细胞瘤的进展[3]。
此外,铜死亡相关基因与肿瘤微环境之间也具有相关性,铜还可以调节 PD-L1 的表达,这为铜死亡与肿瘤免疫疗法提供了新的思路。
本期小 M 为大家介绍了铜在人体的正常代谢,铜死亡作为一种新的死亡方式与其他细胞死亡的区别,铜死亡与癌症的联系及临床研究现状。是不是让您对铜死亡有了更进一步的了解~关注收藏,不要辜负小 M 的用心整理哦~