自2013年以来,“低内毒素回收”(LER)现象在细菌内毒素检测领域引起了广泛关注。LER描述了在含有螯合缓冲液和聚山梨醇酯的未稀释单克隆抗体制剂中,观察到的鲎试剂(LAL)检测干扰(抑制)。这一现象引发了关于病患者安全和药典细菌内毒素测试在检测生物制品中低水平内毒素污染有效性方面的广泛讨论。

一、内毒素与LPS的基本概念
在讨论LER现象时,首先需要明确“内毒素”和“脂多糖”(LPS)的概念。
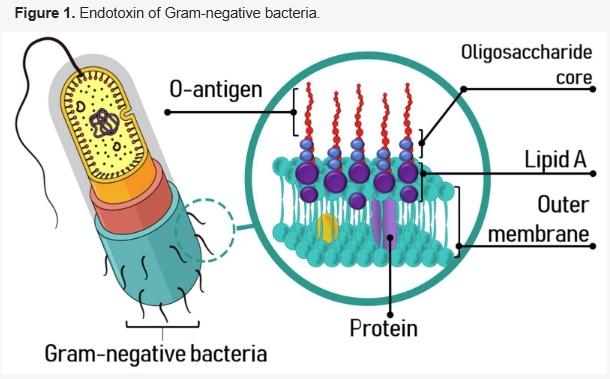
内毒素是革兰氏阴性细菌外细胞膜的成分,而LPS是内毒素复合物的特定成分,包括脂质A部分,它会引起哺乳动物的致热反应,并在LAL测试中引发信号产生。LPS是一种两亲性分子,其疏水部分(脂质A)嵌入细胞膜,亲水部分(O抗原)暴露于细胞外环境。
二、LER现象的生化与物理基础
美国药典(USP)内毒素参考标准品(RSE)和目前与LAL检测试剂盒相关的所有市售内毒素控制标准品(CSE)都是从各种大肠杆菌菌株中提取和纯化的“裸”LPS制剂。
在LAL试验中,RSE和CSE的剧烈混合是为了确保溶解材料的适当再悬浮,防止LPS吸附在容器表面,并优化LPS的聚集状态以进行试验。然而,在LER制剂中,螯合剂和聚山梨醇酯会导致LPS聚集体变小,甚至接近单体状态,进而降低其生物活性,出现LER现象。
三、LER现象对患者安全与药典测试的影响
LER现象可能导致LAL检测出现假阴性结果,从而对患者安全构成隐患。然而,经过改进的工艺控制加上有效的LAL检测,在工艺过程和释放检测中都很好地保证了这些生物制剂的供应安全。
此外,欧盟委员会(EC)和美国药典(USP)的专家委员会也对LER现象进行了深入研究,并认为当前的药典测试方法对于检测生物制品中的内毒素污染是有效的。
四、LER现象的实验研究与数据支持
多项实验研究表明,LER现象并不是LAL测试有效性的问题,而是用作对照的加标分析物的选择以及保持时间研究的实验设计的问题。
例如,在一项LER制剂保持时间研究中,同时进行了兔子热原测试(RPT)和LAL检测,并使用内毒素参考标准品(RSE)和各种实验室衍生的囊泡制剂(如阴沟肠杆菌、皮氏罗尔斯顿氏菌、大肠杆菌、铜绿假单胞菌和粘质沙雷氏菌)作为加标分析物。在研究开始时(T=0),所有加标制剂在RPT中产生类似热原反应,且在LAL试验中完全检测到。在保持24小时后,囊泡制剂在RPT中仍有反应,LAL检测回收正常;但RSE在兔热原试验和LAL检测中均无反应,显示了LER现象的存在。
此外,已发表的数据也表明,在适当的实验条件下,使用天然内毒素囊泡作为分析物可以克服用RSE或CSE观察到的LER效应。
五、总结
LER现象揭示了LPS和内毒素虽然在化学、结构和物理上存在差异,但都可能引起相似的反应。因此,在使用“内毒素”一词时,必须明确其含义。此外,针对LER现象的研究也促使USP提出了一种由天然内毒素组成的新型“天然内毒素”(NOE)标准制剂,以更好地模拟天然内毒素污染的情况,并进一步提高LAL检测的准确性。
LER现象是一个复杂的问题,涉及多个方面的因素。然而,经过深入研究和实践验证,当前的LAL检测方法在检测生物制品中的内毒素污染方面仍然是有效的。未来,随着对LER现象和NOE标准制剂的进一步研究,我们将有望进一步提高内毒素检测的准确性和可靠性。