介绍
近期,浙江大学医学院传染病诊治国家重点实验室刁宏燕老师课题组于2024年3月24 日发表在Molecular Cancer Research (IF:5.2)上题为“Hepatitis B Virus-mediated m6A demethylation increases hepatocellular carcinoma stemness and immune escape”的文章,借助肝细胞癌模型(HCC)及多种技术揭示了HBV通过在ALKBH5-YTHDF2依赖的条件下提高SNAI2的m6A修饰,促进HCC干细胞样表型的维持,并增加免疫检查点受体CD155的表达。
摘要
乙型肝炎病毒(HBV)持续感染在肝细胞癌(HCC)肿瘤发生中起着重要作用。许多研究揭示了多种癌症中N6-甲基腺苷(m6A)的关键作用,而HBV持续感染相关HCC中m6A的调节机制尚未阐明。在这里,课题组通过增强ALKBH5 mRNA的稳定性,证明HBV在HBV阳性HCC中下调m6A修饰水平。更具体地说,课题组还发现ALKBH5 mRNA在HBV阳性HCC的干细胞维持和自我更新中是必需的,但在HBV阴性HCC中是不必要的。机制上,ALKBH5去除了SNAI2基因30个未翻译区(UTR)的m6A修饰,防止YTHDF2在那里被识别,从而稳定SNAI2转录本,从而促进HBV阳性HCC中的癌干细胞特性。此外,SNAI2的表达逆转了降低ALKBH5后抑制干细胞特性的作用。此外,ALKBH5/SNAI2轴通过激活免疫检查点受体CD155来加速肿瘤免疫逃避。课题组的研究揭示了ALKBH5作为HBV相关HCC的关键调节因子,能够诱导SNAI2的m6A去甲基化,并鉴定了ALKBH5/SNAI2/YTHDF2轴在HBV感染过程中促进干细胞样表型和免疫逃逸的功能。
材料和方法
细胞培养和组织标本获取(HCC cells、Mouse Hepa1-6 cell line、NK-92MI cells)、PDX造模(HepG2.215 cells 和Hep3B cells)、Western blot分析、肿瘤球培养、多重免疫组化和定量分析、肝细胞癌类器官构建(HCC)、MeRIP-seq数据分析、NK-92MI细胞杀伤实验、IHC和评分、统计分析。
结果
1、hbv阳性HCC细胞中m6A水平降低可增强干性维持
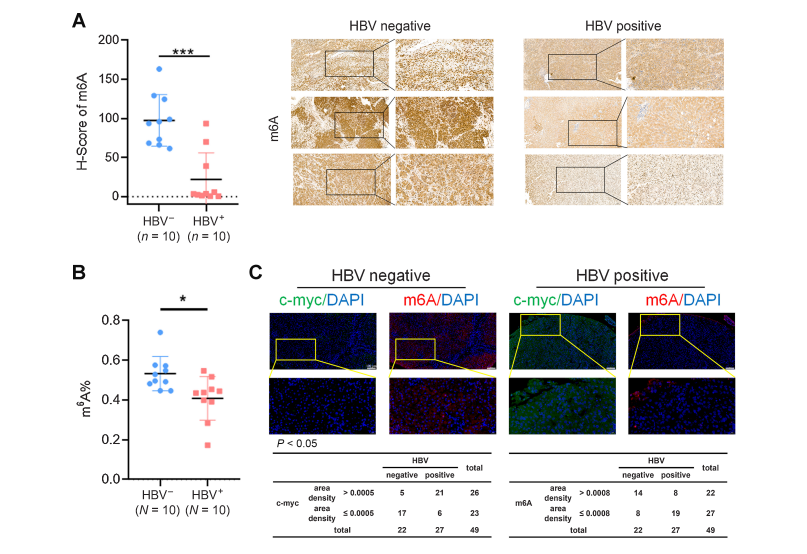
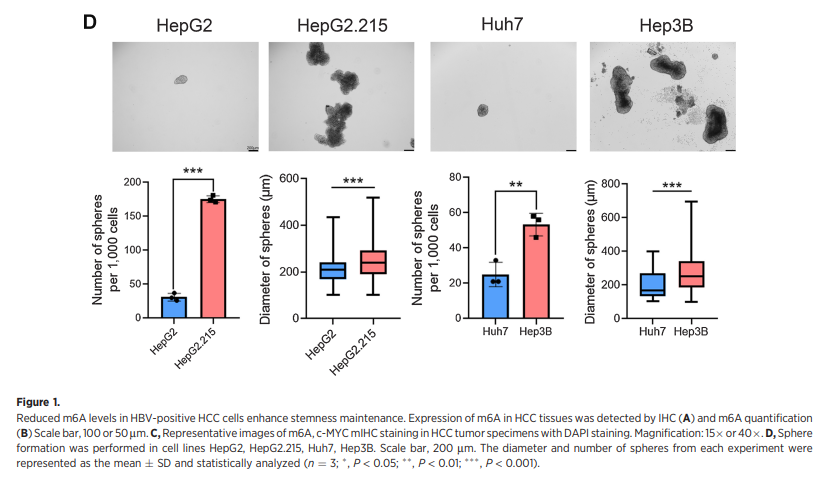
2、HBV增强ALKBH5 mRNA稳定性,促进干细胞样特性
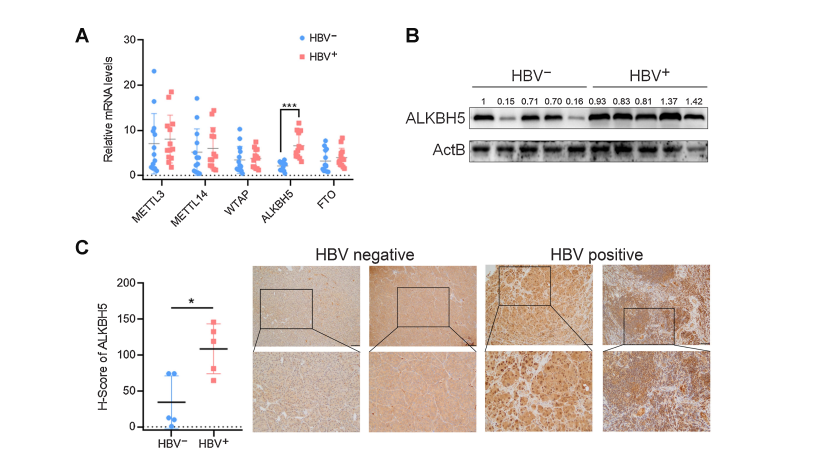
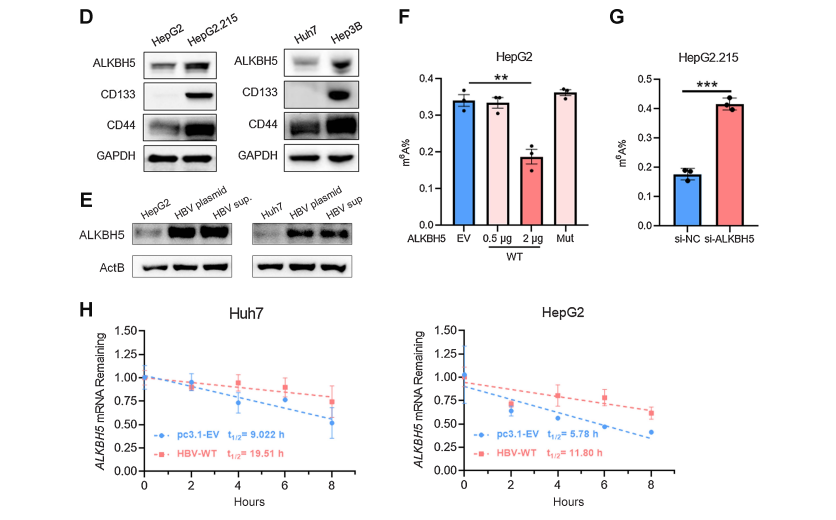

3、在hbv阳性HCC中,ALKBH5是维持肝癌细胞自我更新所必需的因素
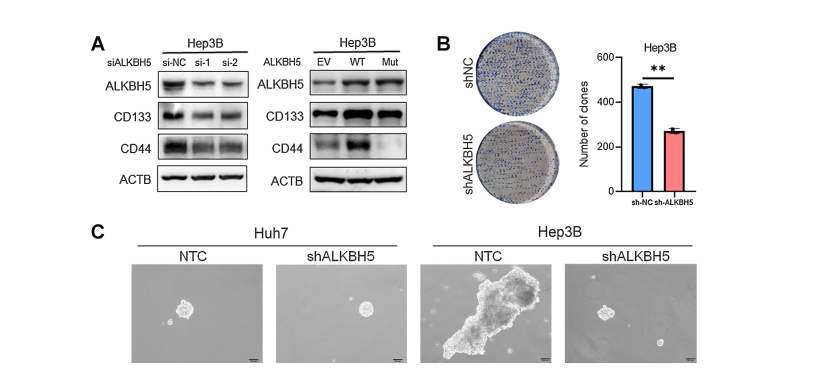
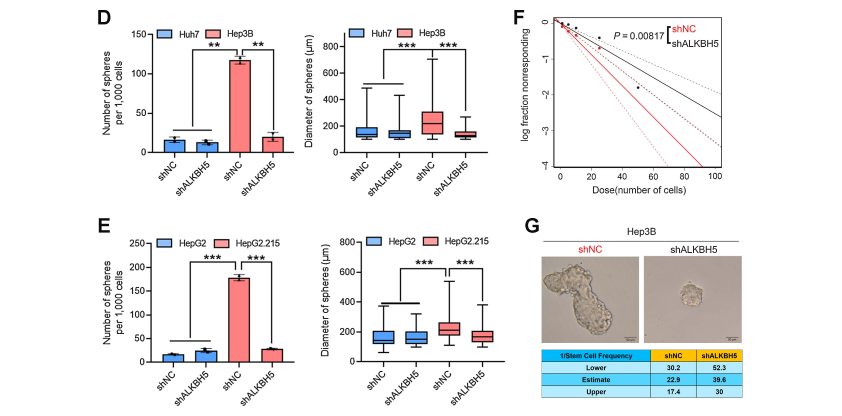
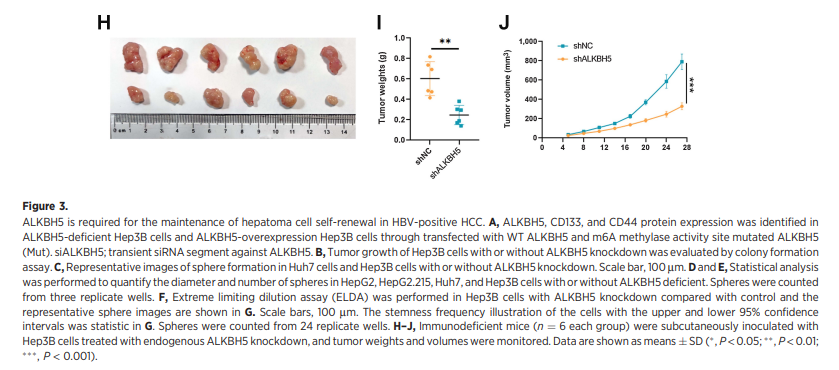
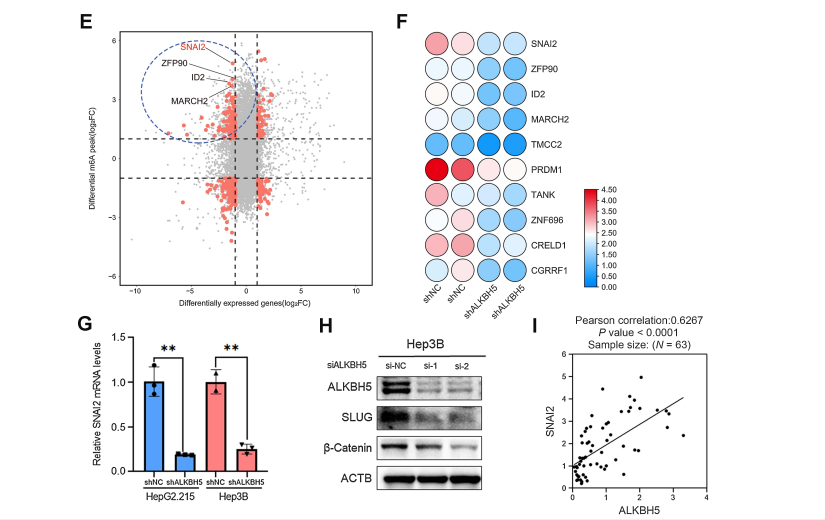
4、SNAI2是hbv阳性HCC中ALKBH5功能上重要的靶基因
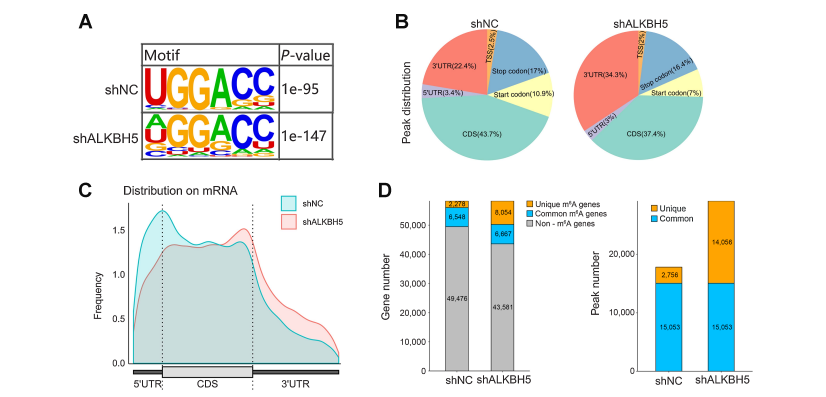

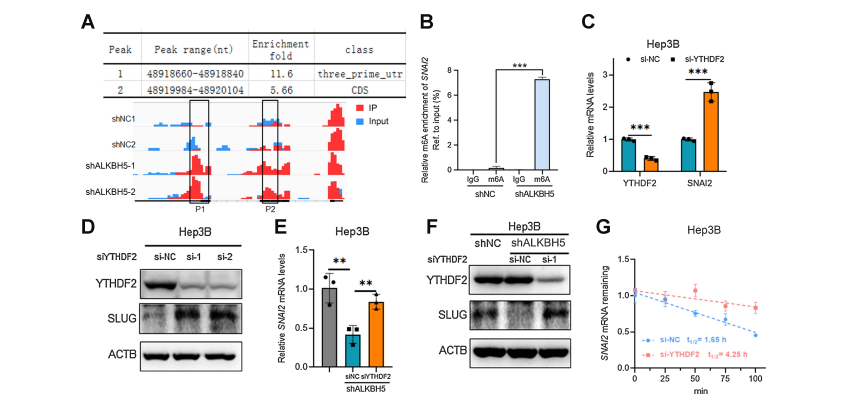
5、30 UTR中alkbh5介导的m6A去甲基化通过ythdf2依赖途径稳定SNAI2 mRNA水平
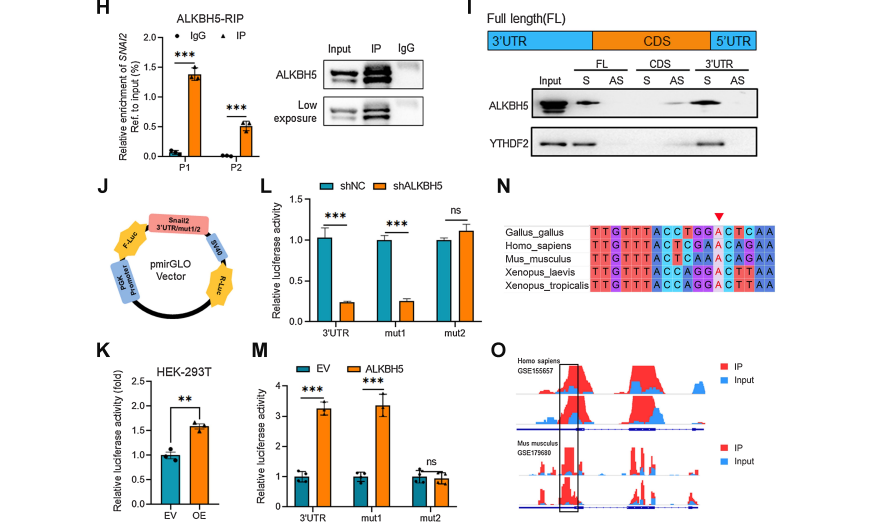

6、SLUG参与alkbh5调控的hbv相关HCC的干细胞样特性
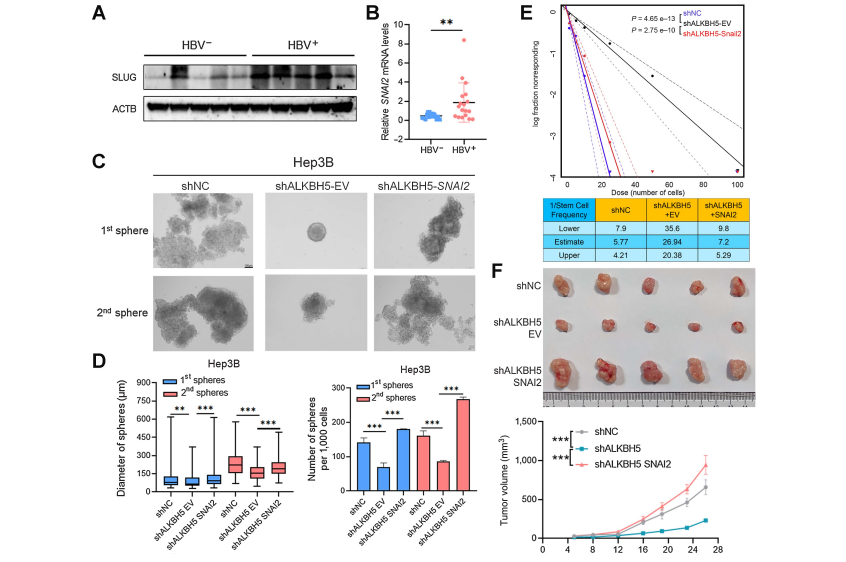
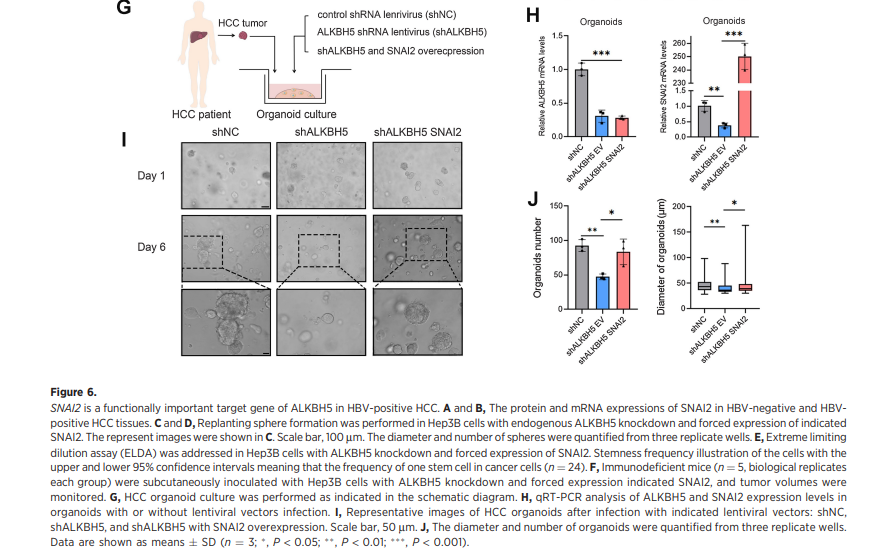
7、LKBH5/SNAI2轴通过调节CD155促进肿瘤免疫逃避
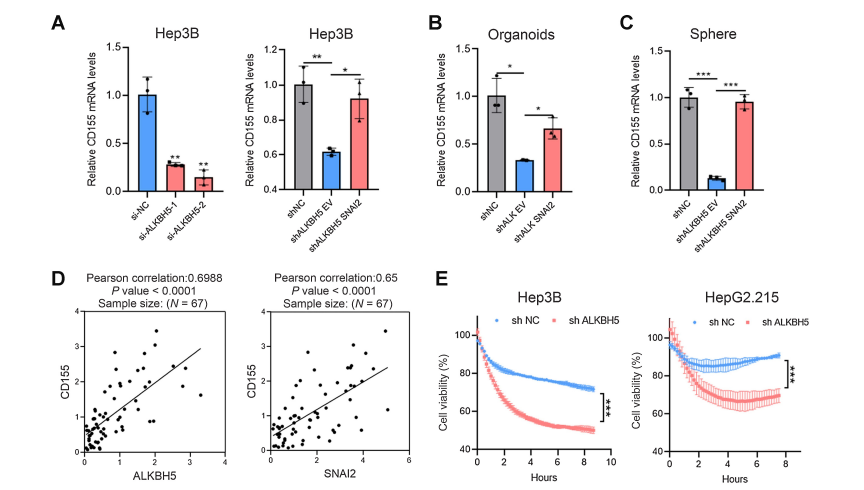
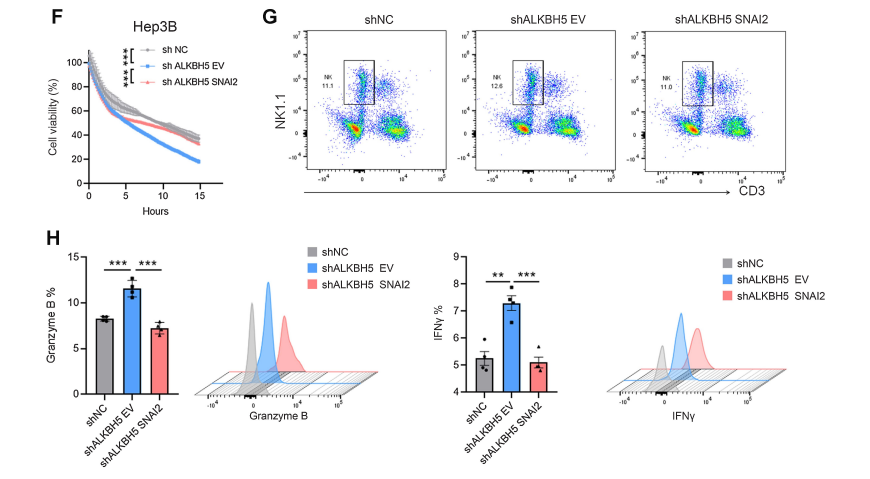

结论
总的来说,课题组的结果显示ALKBH5与SNAI2的转录物3'UTR互作进一步去甲基化m6A修饰,增强了SNAI2的稳定性以维持其高表达和促进HBV相关HCC的干性维持和免疫逃逸。精确靶向ALKBH5的表达对hbv相关HCC的治疗是至关重要的方法。
文献地址:https://doi.org/10.1158/1541-7786.MCR-23-0720
类器官培养相关产品