寡核苷酸合成是许多分子生物学应用的基础,包括聚合酶链反应 (PCR)、基因编辑、DNA 测序和基因治疗。寡核苷酸主要是用固相合成方法制造的。目前,固相合成方法已经发展到允许合成数公斤数量的寡核苷酸用作药物分子 (如反义寡核苷酸)。固相化学合成是由 Robert Bruce Merrifield 在 20 世纪 60 年代发明的,其重要性使得他在 1984 年获得了诺贝尔化学奖。此外,固相合成方法也广泛应用于多肽合成、寡糖合成和组合化学等领域。

寡核苷酸是通过磷酸二酯基团连接在一起的核苷类线性聚合物。想要了解寡核苷酸合成过程,首先需要了解它的组成单体核苷酸和核苷的结构。
核苷由一个碱基和一个糖组成。核苷酸则有一个额外的磷酸基。核苷、核苷酸和五个天然碱基的结构如图 1 所示[1]。通过磷酸二酯基团连接将一个核苷的 3'-羟基连接到下一个核苷的 5'‐羟基,从而形成核酸链。


图 1. 核苷酸、核苷和碱基的结构[1]。

▐ 寡核苷酸引物和探针
合成寡核苷酸最普遍的用途是用作探针和引物。作为引物,寡核苷酸通常用于引发酶促反应,以生成短或长靶序列的数百万至数十亿个副本。众所周知的例子是聚合酶链式反应 (PCR) 或 Sanger 测序方法。寡核苷酸引物的应用包括 DNA 测序、基因表达 (Real Time PCR)、基因克隆和分子诊断。作为探针,寡核苷酸用于鉴定以及结合特定的 DNA 或 RNA 靶序列,以确认该序列在特定样本中的存在。使用寡核苷酸探针的应用包括 Northern 印迹 (用于 RNA),Southern 印迹 (用于 DNA),或荧光原位杂交技术 (FISH,可以检测结合了荧光探针的 DNA 区域或 RNA 在染色体或其他细胞器中的定位)。
目前就有文章报道可以利用设计的 FISH 探针 (CoronaFISH) 可视化新冠病毒SARS-CoV-2 的 RNA (图 2),作为微阵列中的荧光基团偶联序列,可检测基因表达的变化,或者用于筛选遗传疾病或鉴定特定病原体 (分子诊断)。

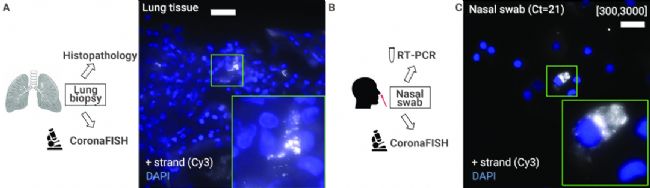
图 2. 人组织和鼻拭子中的新冠病毒[2]。
此外,核酸适配体荧光探针利用核酸适配体与靶分子的高亲和性对活细胞甚至是亚细胞结构 (如 RNA、代谢物、蛋白等) 进行荧光成像分析 (图 3)。

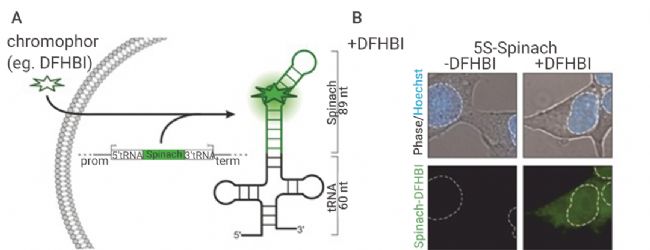
图 3. 荧光核酸适配体发光示意图[3]。
▐ 寡核苷酸治疗/基因治疗
在治疗应用中,反义寡核苷酸 (Antisense oligonucleotides, ASOs),小干扰 RNA (Small interference RNA, siRNA),微小 RNA (Micro-RNA, miRNA) 和核酸适配体 (Aptamers) 等可以通过碱基互补配对原则与 DNA、mRNA 或者 pre-mRNA 配对,并通过一系列过程调节基因表达,如 RNA 干扰,RNase H 介导的靶基因降解和剪接调制等[4]。寡核苷酸疗法在精确医疗方面的潜力激发了人们将寡核苷酸药物应用于癌症、心血管疾病和罕见疾病治疗的热情。目前,涉及多个疾病领域的 18 种寡核苷酸类药物 (包含退市药物) 已获得批准上市。
表 1. 已批准上市的寡核苷酸药物[1][2]。
























固相合成方法是将核苷亚磷酰胺单体按照特定顺序偶联到固体载体上。核苷亚磷酰胺单体是固相合成的构建基块,在合成时将核苷亚磷酰胺单体按照特定顺序偶联到固体载体上。其中 2'/5'-OH 和杂环氨基被保护基团保护以防止合成过程中的副反应。图 2 显示了亚磷酰胺单体的结构以及常见的保护基团[1]。保护基团被设计成在不同的 pH 值下选择性地去除。选择性地去除保护基团,使所需要的官能团显露出来,保证了反应选择性的控制。

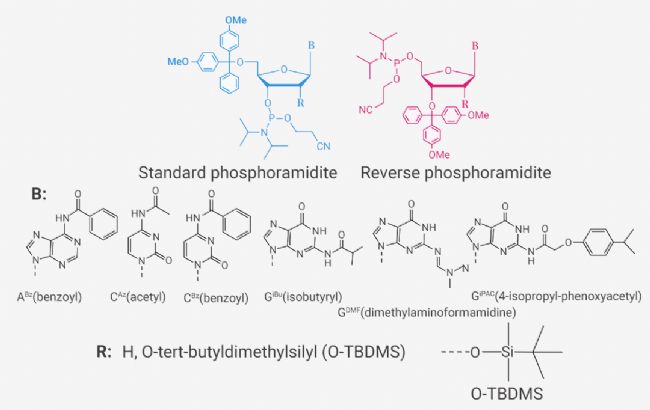
图 4. 核苷亚磷酰胺单体和常用保护基团的结构[1]。

寡核苷酸固相合成方法是一种化学合成方法,一般是从 3' 向 5' 方向进行的,不同于核酸生物合成过程从 5' 向 3' 方向延伸。每个合成周期延长一个核苷酸。
在寡核苷酸合成的开始阶段,第一个受保护的核苷是通过载体表面上的羟基或氨基官能团被预先连接到固相载体上。在合成循环中,寡核苷酸链从第一个被预先固定在固相载体表面上受保护的核苷向后延伸。其中,固体载体 (也称为树脂) 是不溶性颗粒,通常直径为 50-200 μm,广泛采用的固相载体是可控微孔玻璃 (CPG) 和聚苯乙烯 (PS) 两类载体。试剂被泵入并流经固相载体表面,诱导分步添加的核苷酸单体加入到寡核苷酸链上,使寡核苷酸链不断延长。反应步骤包括:1. 脱保护基团 (Detritylation),2. 活化和偶联 (Activation and Coupling),3. 氧化 (Oxidation),4. 加帽 (Capping)。


图 5. 寡核苷酸的固相合成过程[1]。
1. 脱保护基团:在寡核苷酸合成之前,用三氯乙酸 (TCA) 脱去连接在固相载体上的核苷 5'-DMT 保护基团,获得游离的 5'-OH 基团,以供下一步缩合反应。2. 活化和偶联:将过量核苷亚磷酰胺单体与四氮唑活化剂混合并进入合成柱,核苷亚磷酰胺单体的二异丙基氨基团被活化剂质子化,与游离的 5'-OH 发生亲和反应,缩合并脱去四唑,从而形成磷酸三酯键,此时合成的寡核苷酸链延长一个碱基。3. 氧化:在偶联反应过程中形成的亚磷酸三酯是不稳定的,必须在下一个循环开始之前将其转化为更稳定的结构。需要氧化试剂将亚磷酸三酯转化为稳定的磷酸三酯。最常使用的氧化试剂是碘溶于四氢呋喃/吡啶/水的溶液。所得磷酸三酯是由 2-氰基乙基保护。氰基乙基基团防止后续合成循环中磷酸三酯发生其他反应。偶联步骤对水分敏感,在下一次偶联之前,必须用乙腈洗涤除去残留的水。4. 加帽:加入的核苷亚磷酰胺单体与预先连接在载体上的核苷无法实现 100% 的反应。这意味着预先连接在载体上的核苷仍然会有一些未反应的游离的 5'-OH 基团。如果不加以控制,这些 5'-OH 基团将参与下一个偶联步骤。这样产生的寡核苷酸将缺少一个碱基。因此,需要将剩余的 5'-OH 基团封闭。常用的加帽试剂有乙酸酐和 N -甲基咪唑 (NMI)。之后,每个碱基重复这个循环一次,最终产生所需的寡核苷酸。
近些年发展了一些修饰试剂,可以在合成寡核苷酸时对于一些核苷进行化学修饰。许多化学修饰可以改善寡核苷酸的药代动力学特性、耐受性和靶向结合亲和力。硫代磷酸 (PS)、磷酸二酰胺吗啉基 (PMO) 和肽核酸 (PNA) 设计都赋予了对核酸酶的抵抗力和细胞内增强摄取能力,从而增加了寡核苷酸的效力。tcDNA 是构象受限的 DNA 类似物,在全身给药后在组织中具有增强的效力和摄取能力。此外,在核糖的 2ʹ 位置进行的修饰包括 2'-O-甲基 (2'-OMe)、2'-O-甲氧乙基 (2'-MOE) 和锁核酸 (LNA) 使寡核苷酸更耐核酸酶降解,进一步增加稳定性,还提高了其与靶基因的亲和力,减少了非特异性蛋白结合带来的毒性[4][5]。

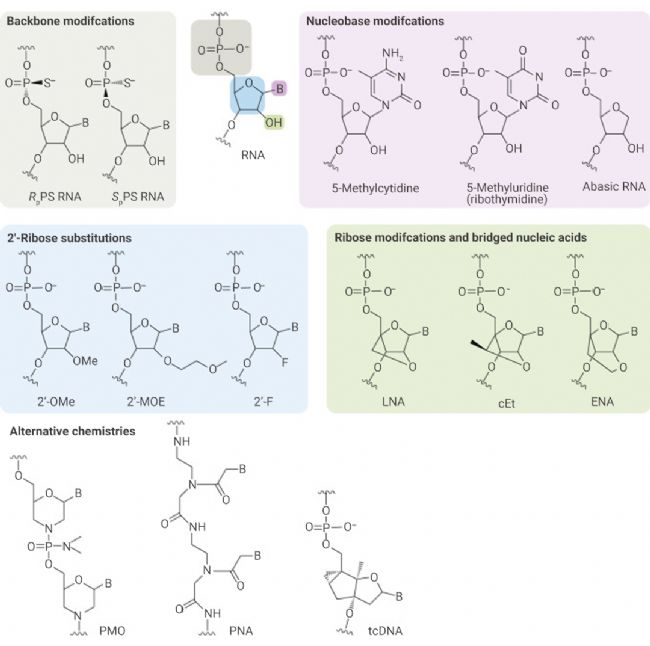
图 6. 常见的寡核苷酸化学修饰[4]。
MCE 拥有专业的研发团队和先进的检测设备,可提供寡核苷酸相关产品的定制合成服务,进行相关的检测服务(纯度、结构和稳定性分析等),确保产品的有效性与一致性,提供优质高效的服务品质。
相关服务
• siRNA 合成:提供单基因套装 (3 保 1) 和 siRNA 文库。
• miRNA 合成:提供 miRNA mimics 和 miRNA inhibitors 文库。
• 引物/基因定制合成:支持提供多样的化学修饰 (如锁核酸 LNA,硫代磷酸化,氟代,2’-OMe,2’-MOE 等) 和荧光标记 (CY3,CY5,和 FAM 等)。
• 寡核苷酸偶联:可偶联 PEG、脂质、小分子化合物、或多肽等。


[1] Pourshahian S. THERAPEUTIC OLIGONUCLEOTIDES, IMPURITIES, DEGRADANTS, AND THEIR CHARACTERIZATION BY MASS SPECTROMETRY. Mass Spectrom Rev. 2021;40(2):75-109.
[2] Rensen E, et al. Sensitive visualization of SARS-CoV-2 RNA with CoronaFISH. Life Sci Alliance. 2022;5(4):e202101124.
[3] Neubacher S, et al. RNA Structure and Cellular Applications of Fluorescent Light-Up Aptamers. Angew Chem Int Ed Engl. 2019;58(5):1266-1279.
[4] Roberts TC, et al. Advances in oligonucleotide drug delivery. Nat Rev Drug Discov. 2020;19(10):673-694.
[5] Rinaldi C, et al. Antisense oligonucleotides: the next frontier for treatment of neurological disorders. Nat Rev Neurol. 2018;14(1):9-21.