血管造影OCT能够区分小鼠皮下表达不同VEGF亚基的纤维肉瘤的血管模式
来宝网 2022/8/11点击3145次
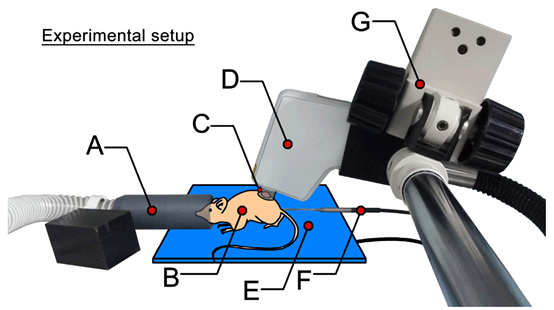
小鼠皮下植入肿瘤模型常用于癌症研究,尽管肿瘤植入的位置很浅,但对于微血管研究来说,以足够的空间分辨率进行无创成像仍然是一个难题。英国谢菲尔德大学的研究人员Robert
A.
Byers等评估了使用OCT血管造影术直接对这种小鼠模型中肿瘤血管成像的能力。使用的肿瘤来源于纤维肉瘤细胞,经基因工程改造后仅表达VEGF120或VEGF188(分别为fs120和fs188肿瘤)。研究发现fs120肿瘤的血管直径(60.7
± 4.9 μm)显著大于fs188肿瘤(45.0 ± 4.0
μm)。fs120肿瘤还显示出明显更高的血管弯曲度、分形维数和密度。为观察皮下肿瘤微循环的纵向动力学提供了一种可靠、无创的方法。研究成果以“Vascular
patterning of subcutaneous mouse fibrosarcomas expressingindividual
VEGF isoforms can be differentiated using angiographic opticalcoherence
tomography”为题发表于Biomedical Optics EXPRESS。
背景
生物体中,主要动脉和静脉的结构特征受遗传控制,通常在个体间保持一致。然而微血管系统则会受到局部微环境中分子和机械刺激而发生动态重塑。肿瘤的生长依赖于持续的微血管化过程,特别是通过血管生成,这也促进了肿瘤的转移,由此产生的肿瘤脉管系统在形态和功能上都是异常的,研究肿瘤的脉管系统可能为肿瘤的发展和病理生理学提供很有价值的信息。
利用小鼠癌症模型进行的血管造影成像研究在肿瘤学研究中特别重要,能大大有助于我们了解肿瘤的生长、进展和活体动物的治疗。而传统的尸检方法如免疫组织化学,仍在量化植入肿瘤内的微循环中占重要地位。非侵入性成像技术由于纵向血管可视化的潜力很快获得了发展,大大减少了产生统计可靠数据所需的动物数量。目前,活体显微技术被广泛用于研究肿瘤生长,通常包括用透明玻璃盖玻片对高度散射的皮肤层进行手术置换。使用该模型,血管造影OCT成像已被用于实现肿瘤动力学和治疗反应的高分辨率纵向成像。此外,通过灌注计算机断层扫描和动态磁共振成像,已经实现对皮下生长肿瘤的体内全视野血管造影,同时覆盖的皮肤完好无损。最近,多光谱光声断层扫描已被用于可视化1 cm3肿瘤体积中的血管形态和氧合,分辨率达70 μm。
尽管取得了这些进展,但对皮下植入肿瘤内的微循环(通常直径为5-50 μm)进行非侵入性成像仍然具有难度,因为成像所用的光学模式通常无法穿透皮肤的高度散射层。OCT已被广泛用于捕捉人体皮肤内的结构和血管造影图像。最值得注意的是,OCT在组织内的穿透深度可达约1 mm,并能够提取深度编码数据,从而可以以高分辨率可视化组织的各个层。相比于几毫米厚的人皮肤,雌性CD-1裸鼠浅表组织通常约550 μm厚(~30 μm表皮,~220 μm真皮,~300 μm皮下),因此皮下植入肿瘤的表面脉管系统是可见的,并且在OCT的视野内。散斑方差OCT(svOCT)可用于从四维OCT数据集(X-Y-Z-Time)中提取流动信息,在每个空间位置收集多个数据点。这是基于这样一个事实,即与固体组织像素相比,流体像素将在OCT信号(散斑模式)中显示快速演变的时间变化。因此,通过计算同一空间位置像素的方差作为时间的函数,在静止固体和运动液体之间产生对比度。
本研究旨在开发和评估血管造影svOCT在小鼠皮下肿瘤成像中的应用及性能。试图区分小鼠肿瘤内的血管形态,这些肿瘤来源于基因工程化的纤维肉瘤细胞,仅表达血管内皮生长因子的单一剪接变异体亚型;VEGF120或VEGF188(分别为fs120和fs188肿瘤)。以前,使用在植入小鼠背部的透明小室中生长的肿瘤和常规活体光学显微镜,我们观察到与fs188肿瘤相比,fs120肿瘤血管更大、更杂乱,并形成更曲折的血管网络。这项研究旨在确定这些不同的血管模式在皮下生长肿瘤的微循环中是否也存在,是否存在普遍性,并不仅限于褶皱窗室模型中。
结果
01-表达VEGF120和188的肿瘤的目视检查
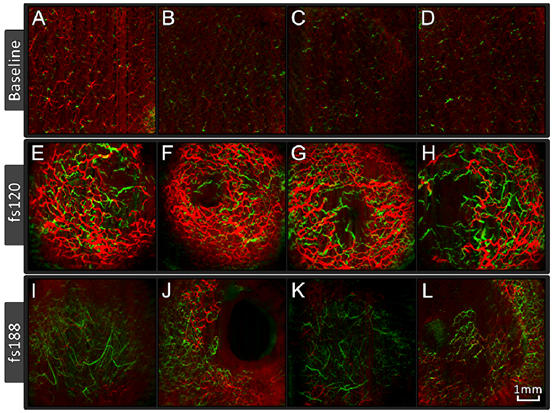
图4为CD1裸鼠对照皮肤和皮下植入肿瘤皮肤的en-face svOCT图像,带有深度编码信息。使用svOCT时大的异常血管网在只能在植入后约8-15天可见(图4E-L),在此之前可见的是更规则的有组织的血管网络(图4A-D)。表明肿瘤血管发育的早期阶段,血管处在组织更深层,无法通过OCT成像。然而肿瘤充分扩张后,通常在植入后约10天,OCT系统视野内可以清楚地看到大的异常血管。后期扫描中除了较大的异常血管外,0-400 μm处的血管造影信号相对较低,意味着似乎没有观察到类似基线脉管系统的结构,表明随着皮肤在肿瘤表面上伸展,正常血管中的血流停止。此外,fs120肿瘤似乎比fs188更具浸润性,血管大部分呈红色(0-400 μm深度),而fs188大部分血管呈绿色(400-800 μm)。这可能与细胞的独特表型有关,无论是体外或体内研究中,fs120细胞都比fs188表现出更强的增殖表型。本研究中svOCT技术有一个局限性,在检测到的血管下观察到阴影效应,这是由血液对光子的前向散射引起的,会遮挡下面的脉管系统。就fs120肿瘤而言,许多可能位于400-800 μm深度(绿色)的血管被0-400 μm深度(红色)的浅表血管遮挡住了,这使得在同等深度进行血管密度计算具有一定难度。
无创皮下肿瘤成像的一个关键优势是能对肿瘤生长和血管发育进行纵向观察。图5为纵向数据采集举例,在5天的时间内分别采集同一个fs120和fs188肿瘤的图像。对fs188肿瘤内血管发育进行了从第0天到第15天的长时间可视化。
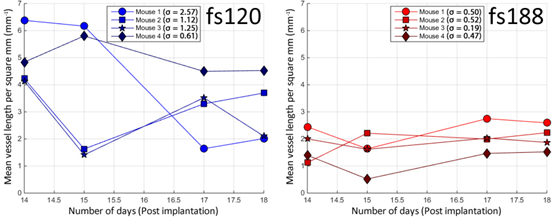
fs120肿瘤中,每平方毫米的平均血管长度在植入后第14天达到最高(4.1 mm-1),然后第15天降至1.4 mm-1,第17天恢复至3.5 mm-1,随后第18天再次降至2.1 mm-1。相比之下fs188肿瘤中,平均血管长度从第14天的1.1 mm-1增加到第15天的2.2 mm-1,第17天减少到2.0 mm-1,随后第18天恢复到2.2 mm-1。计算植入后14至18天内,两组肿瘤中每平方毫米平均血管长度的标准差,用t检验评估显著性。除去不合适的数据,最终可行数据集的数量n = 4。虽然与fs188组(SD = 0.4 mm-1)相比,fs120组的血管长度随时间的变化更大(SD = 1.4 mm-1),但由于样本数量少,该结果在统计学上并不显著(p = 0.063)。因此尚不能确定fs120肿瘤平均血管长度是否确实是每天变化较大。图6为每只动物每平方毫米平均血管长度随时间的变化。
血管数量每天的变化不太可能是血管重塑造成的,可能是塑料支撑帽对皮肤产生的压力,或者血管连接内的局部血流减少到OCT系统的帧采集间隔(~ 30ms)以下,血流信号丧失。此外当该区域对温度等外部刺激的微小变化做出稳态反应时,也可能会引发血管收缩或上游血管分流导致血管不可见。本研究使用的异氟醚麻醉剂也很可能既影响体温调节抑制的程度,又作为心血管抑制剂,降低血压。
03-OCT深度穿透评估
图7为从CD1裸鼠背部采集的OCT B-scan与组织学样本的比较。健康皮肤(图7A,B)中,厚厚的皮下层(约400 μm)填充有密集的毛囊,毛囊会散射入射的1300 nm OCT光束,阻止光穿透到组织深处。OCT图像的右侧可以看到一部分薄薄的横纹肌层,但这层下的结构看不到。
已知鼠皮肤内皮下组织的厚度受毛发周期调节,但肿瘤的存在明显改变了外部皮肤形态(图7C,E)。考虑到皮下组织在横截面OCT图像上的对比度变化,选择组织切片进行皮下组织厚度的测量研究。使用MATLAB手动跟踪皮下组织的上层和下层,然后结合上下层边界之间的垂直距离来计算皮下组织厚度的平均值。对比健康皮肤(n = 7)与研究结束时fs188和fs120肿瘤(每组n = 7)周围皮肤中的皮下组织厚度,在三组间进行单因素方差分析,HSD检验以评估显著性,结果总结在图8中。
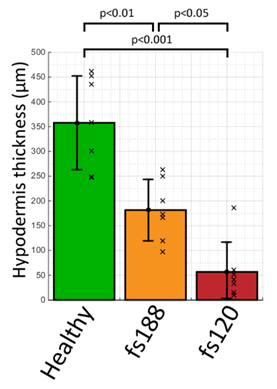
健康皮肤的皮下组织(357 ± 94 μm)明显比fs188组(182 ± 62 μm,p<0.01)和fs120组(57 ± 60 μm,p<0.001)的皮下组织厚。fs188和fs120组中皮肤的厚度显著减少(p = 0.015)可能是由皮肤在生长的肿瘤上伸展时受到异常应力引起的。fs188肿瘤中可观察到皮下组织变薄(图7E,F),OCT能够捕获皮肤的上层(表皮、真皮)、脂肪层(皮下组织)、肌肉层及肿瘤内约500 μm深处,总穿透深度约1 mm。在fs120肿瘤组中,大多数皮肤形态比较特殊,因为缺乏横纹肌层,在一些极端情况下皮下组织也受到严重破坏,脂肪细胞分散在肿瘤内,皮下组织中也明显缺乏毛囊(图7C),再次证明fs120肿瘤可能更具侵袭性。在fs120这种情况下,浅表皮肤的剩余层厚约200 μm,仅由表皮、真皮和极薄的皮下组织构成,因此OCT能观察肿瘤组织更深处(图7D),这可能解释了为什么在小于300 μm的表面深度处可以看到大的异常肿瘤脉管系统(图4)。
图9为健康、fs120和fs188皮肤的H&E和CD31染色切片之间的比较。健康皮肤中(图9A、D、G),CD31免疫染色显示小鼠皮肤的整个真皮、皮下组织和横纹肌层中存在血管内皮细胞。红色箭头所示为最大的可见血管腔,直径约15 μm。在含fs120肿瘤的皮肤中(图9B、E、H),肿瘤周边大部分血管都可见,最大的直径约65 μm(红色箭头)。在含fs188肿瘤的皮肤中(图9C、F、I),真皮/皮下组织内仍有血管形成的证据,但是大多数可见血管位于肿瘤内部,位于深度约为600 μm的横纹肌层正下方,最大直径约50 μm(红色箭头)。
一般来说,该系统的穿透深度足以捕获fs120和fs188肿瘤内的浅层脉管系统,但在某些特定位置,轴向深度穿透仍取决于上皮层中是否存在高散射结构。图7B、D、F中可见表面散射结构(如毛囊)的带状阴影,这些阴影可能会遮挡正下方血管的血管造影信号。
04-定量血管度量
血管造影图像二值化产生血管骨架,从而定量血管参数。结果发现,fs120肿瘤(60.7 ± 4.9 μm)的平均血管直径明显高于fs188肿瘤(45.0 ± 4.0 μm),与之前使用窗室模型的活体观察研究结果一致。Vakoc等人已经证明了窗室模型成像的背景下对于大血管,多光子显微术和OCT血管造影之间具有良好相关性,但对直径小于12 μm的毛细管相关性较差。考虑到fs188肿瘤血管形态较薄,对fs188平均血管直径测量的影响可能比对fs120更大,但不同肿瘤类型之间的差异仍然显著。
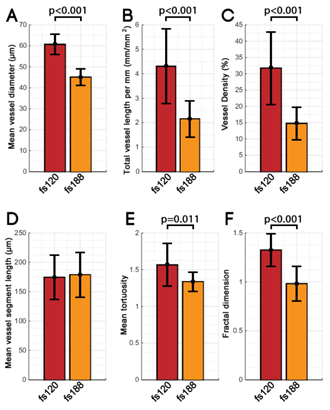
图10. fs120肿瘤(n = 9)和fs188肿瘤(n = 8)间定量血管参数的变化。
fs120肿瘤每平方毫米的总血管长度(4.3 ± 1.5 mm-1)明显大于fs188(2.2 ± 0.7 mm-1),fs120肿瘤的总血管密度(31.7 ± 11.1%)也比fs188肿瘤(14.8 ± 5.0%)高,与之前研究得到的密度计算值一致。而之前的窗室模型中得到的结果与此相反,fs120肿瘤每平方毫米总血管长度较低。这很可能是不同深度或量化方法造成的。事实上由于fs188肿瘤浸润性较弱,脉管系统处于较表层皮肤中,而本所用文骨架化是在0-800 μm的大深度范围内进行的,这将直接导致检测到的整个fs188脉管系统的长度减少。但相同组织深度直接比较,fs120中深处血管又会被浅表血管的阴影所遮挡,产生不准确结果。因此本研究只考虑前100 μm的可见脉管系统,将脉管系统与组织深度分离,得出的fs120肿瘤每平方毫米血管长度(1.5 ± 0.7 mm-1)显著低于(p = 0.04)fs188肿瘤(2.2 ± 0.3 mm-1)。仍不能确认诸如总血管长度/密度之类的深度相关度量是否可靠。
不同肿瘤类型之间平均血管段长度没有显著差异,与之前的窗室模型观察结果一致。fs120组中的血管网络的平均弯曲度和分形维数(分别为1.56 ± 0.29和1.33 ± 0.17)都显著高于fs188组(分别为1.33 ± 0.13和0.98 ± 0.18)。考虑到不同肿瘤类型之间的平均血管段长度没有差异,fs120肿瘤中弯曲度较高意味着fs120血管网络的分支点比fs188肿瘤的分支点靠得更近,而不是分支点之间的血管本身更弯曲。这反映在分形维数测量中,fs188s的分形维数较低,表明血管网络更规则、更有组织。这也与之前用活体显微镜对这些肿瘤类型的观察相一致,即fs120血管通常较宽且排列非常混乱,而fs188血管规则排列且均匀狭窄。
总结
背景
生物体中,主要动脉和静脉的结构特征受遗传控制,通常在个体间保持一致。然而微血管系统则会受到局部微环境中分子和机械刺激而发生动态重塑。肿瘤的生长依赖于持续的微血管化过程,特别是通过血管生成,这也促进了肿瘤的转移,由此产生的肿瘤脉管系统在形态和功能上都是异常的,研究肿瘤的脉管系统可能为肿瘤的发展和病理生理学提供很有价值的信息。
利用小鼠癌症模型进行的血管造影成像研究在肿瘤学研究中特别重要,能大大有助于我们了解肿瘤的生长、进展和活体动物的治疗。而传统的尸检方法如免疫组织化学,仍在量化植入肿瘤内的微循环中占重要地位。非侵入性成像技术由于纵向血管可视化的潜力很快获得了发展,大大减少了产生统计可靠数据所需的动物数量。目前,活体显微技术被广泛用于研究肿瘤生长,通常包括用透明玻璃盖玻片对高度散射的皮肤层进行手术置换。使用该模型,血管造影OCT成像已被用于实现肿瘤动力学和治疗反应的高分辨率纵向成像。此外,通过灌注计算机断层扫描和动态磁共振成像,已经实现对皮下生长肿瘤的体内全视野血管造影,同时覆盖的皮肤完好无损。最近,多光谱光声断层扫描已被用于可视化1 cm3肿瘤体积中的血管形态和氧合,分辨率达70 μm。
尽管取得了这些进展,但对皮下植入肿瘤内的微循环(通常直径为5-50 μm)进行非侵入性成像仍然具有难度,因为成像所用的光学模式通常无法穿透皮肤的高度散射层。OCT已被广泛用于捕捉人体皮肤内的结构和血管造影图像。最值得注意的是,OCT在组织内的穿透深度可达约1 mm,并能够提取深度编码数据,从而可以以高分辨率可视化组织的各个层。相比于几毫米厚的人皮肤,雌性CD-1裸鼠浅表组织通常约550 μm厚(~30 μm表皮,~220 μm真皮,~300 μm皮下),因此皮下植入肿瘤的表面脉管系统是可见的,并且在OCT的视野内。散斑方差OCT(svOCT)可用于从四维OCT数据集(X-Y-Z-Time)中提取流动信息,在每个空间位置收集多个数据点。这是基于这样一个事实,即与固体组织像素相比,流体像素将在OCT信号(散斑模式)中显示快速演变的时间变化。因此,通过计算同一空间位置像素的方差作为时间的函数,在静止固体和运动液体之间产生对比度。
本研究旨在开发和评估血管造影svOCT在小鼠皮下肿瘤成像中的应用及性能。试图区分小鼠肿瘤内的血管形态,这些肿瘤来源于基因工程化的纤维肉瘤细胞,仅表达血管内皮生长因子的单一剪接变异体亚型;VEGF120或VEGF188(分别为fs120和fs188肿瘤)。以前,使用在植入小鼠背部的透明小室中生长的肿瘤和常规活体光学显微镜,我们观察到与fs188肿瘤相比,fs120肿瘤血管更大、更杂乱,并形成更曲折的血管网络。这项研究旨在确定这些不同的血管模式在皮下生长肿瘤的微循环中是否也存在,是否存在普遍性,并不仅限于褶皱窗室模型中。
结果
01-表达VEGF120和188的肿瘤的目视检查
图4为CD1裸鼠对照皮肤和皮下植入肿瘤皮肤的en-face svOCT图像,带有深度编码信息。使用svOCT时大的异常血管网在只能在植入后约8-15天可见(图4E-L),在此之前可见的是更规则的有组织的血管网络(图4A-D)。表明肿瘤血管发育的早期阶段,血管处在组织更深层,无法通过OCT成像。然而肿瘤充分扩张后,通常在植入后约10天,OCT系统视野内可以清楚地看到大的异常血管。后期扫描中除了较大的异常血管外,0-400 μm处的血管造影信号相对较低,意味着似乎没有观察到类似基线脉管系统的结构,表明随着皮肤在肿瘤表面上伸展,正常血管中的血流停止。此外,fs120肿瘤似乎比fs188更具浸润性,血管大部分呈红色(0-400 μm深度),而fs188大部分血管呈绿色(400-800 μm)。这可能与细胞的独特表型有关,无论是体外或体内研究中,fs120细胞都比fs188表现出更强的增殖表型。本研究中svOCT技术有一个局限性,在检测到的血管下观察到阴影效应,这是由血液对光子的前向散射引起的,会遮挡下面的脉管系统。就fs120肿瘤而言,许多可能位于400-800 μm深度(绿色)的血管被0-400 μm深度(红色)的浅表血管遮挡住了,这使得在同等深度进行血管密度计算具有一定难度。

图4. en-face svOCT图像。A-D)无肿瘤的基线鼠皮肤脉管系统。E-L)已建立的皮下肿瘤脉管系统。E-H)fs120肿瘤。I-L)fs188肿瘤。所有图像都是从不同的动物身上拍摄的。颜色对应被检测血管的深度,红色在皮肤表面下0-400
μm,绿色在皮肤表面下400-800 μm。
02-纵向肿瘤监测的评估
无创皮下肿瘤成像的一个关键优势是能对肿瘤生长和血管发育进行纵向观察。图5为纵向数据采集举例,在5天的时间内分别采集同一个fs120和fs188肿瘤的图像。对fs188肿瘤内血管发育进行了从第0天到第15天的长时间可视化。
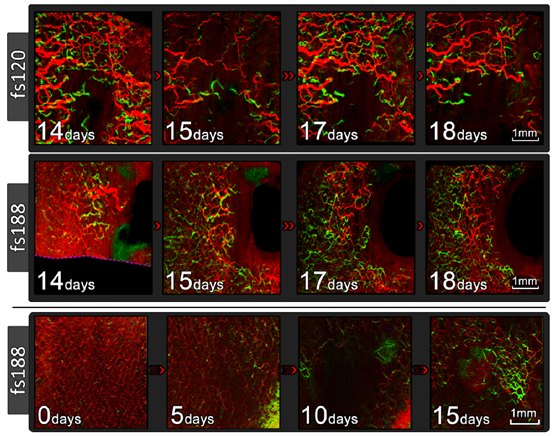
fs120肿瘤中,每平方毫米的平均血管长度在植入后第14天达到最高(4.1 mm-1),然后第15天降至1.4 mm-1,第17天恢复至3.5 mm-1,随后第18天再次降至2.1 mm-1。相比之下fs188肿瘤中,平均血管长度从第14天的1.1 mm-1增加到第15天的2.2 mm-1,第17天减少到2.0 mm-1,随后第18天恢复到2.2 mm-1。计算植入后14至18天内,两组肿瘤中每平方毫米平均血管长度的标准差,用t检验评估显著性。除去不合适的数据,最终可行数据集的数量n = 4。虽然与fs188组(SD = 0.4 mm-1)相比,fs120组的血管长度随时间的变化更大(SD = 1.4 mm-1),但由于样本数量少,该结果在统计学上并不显著(p = 0.063)。因此尚不能确定fs120肿瘤平均血管长度是否确实是每天变化较大。图6为每只动物每平方毫米平均血管长度随时间的变化。

图6 皮下肿瘤内每平方毫米血管长度随时间变化的线图,蓝色为fs120,红色为fs188。
血管数量每天的变化不太可能是血管重塑造成的,可能是塑料支撑帽对皮肤产生的压力,或者血管连接内的局部血流减少到OCT系统的帧采集间隔(~ 30ms)以下,血流信号丧失。此外当该区域对温度等外部刺激的微小变化做出稳态反应时,也可能会引发血管收缩或上游血管分流导致血管不可见。本研究使用的异氟醚麻醉剂也很可能既影响体温调节抑制的程度,又作为心血管抑制剂,降低血压。
03-OCT深度穿透评估
图7为从CD1裸鼠背部采集的OCT B-scan与组织学样本的比较。健康皮肤(图7A,B)中,厚厚的皮下层(约400 μm)填充有密集的毛囊,毛囊会散射入射的1300 nm OCT光束,阻止光穿透到组织深处。OCT图像的右侧可以看到一部分薄薄的横纹肌层,但这层下的结构看不到。
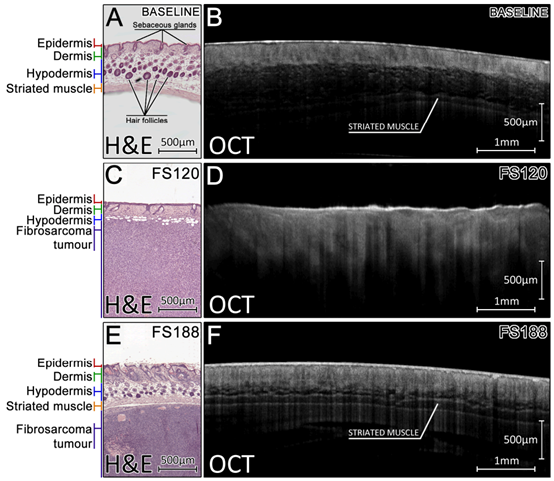
已知鼠皮肤内皮下组织的厚度受毛发周期调节,但肿瘤的存在明显改变了外部皮肤形态(图7C,E)。考虑到皮下组织在横截面OCT图像上的对比度变化,选择组织切片进行皮下组织厚度的测量研究。使用MATLAB手动跟踪皮下组织的上层和下层,然后结合上下层边界之间的垂直距离来计算皮下组织厚度的平均值。对比健康皮肤(n = 7)与研究结束时fs188和fs120肿瘤(每组n = 7)周围皮肤中的皮下组织厚度,在三组间进行单因素方差分析,HSD检验以评估显著性,结果总结在图8中。

图8. 健康皮肤的皮下组织层厚度变化,与包裹着直径约12 mm的fs188和fs120肿瘤的皮肤皮下组织层厚度变化的比较。
健康皮肤的皮下组织(357 ± 94 μm)明显比fs188组(182 ± 62 μm,p<0.01)和fs120组(57 ± 60 μm,p<0.001)的皮下组织厚。fs188和fs120组中皮肤的厚度显著减少(p = 0.015)可能是由皮肤在生长的肿瘤上伸展时受到异常应力引起的。fs188肿瘤中可观察到皮下组织变薄(图7E,F),OCT能够捕获皮肤的上层(表皮、真皮)、脂肪层(皮下组织)、肌肉层及肿瘤内约500 μm深处,总穿透深度约1 mm。在fs120肿瘤组中,大多数皮肤形态比较特殊,因为缺乏横纹肌层,在一些极端情况下皮下组织也受到严重破坏,脂肪细胞分散在肿瘤内,皮下组织中也明显缺乏毛囊(图7C),再次证明fs120肿瘤可能更具侵袭性。在fs120这种情况下,浅表皮肤的剩余层厚约200 μm,仅由表皮、真皮和极薄的皮下组织构成,因此OCT能观察肿瘤组织更深处(图7D),这可能解释了为什么在小于300 μm的表面深度处可以看到大的异常肿瘤脉管系统(图4)。
图9为健康、fs120和fs188皮肤的H&E和CD31染色切片之间的比较。健康皮肤中(图9A、D、G),CD31免疫染色显示小鼠皮肤的整个真皮、皮下组织和横纹肌层中存在血管内皮细胞。红色箭头所示为最大的可见血管腔,直径约15 μm。在含fs120肿瘤的皮肤中(图9B、E、H),肿瘤周边大部分血管都可见,最大的直径约65 μm(红色箭头)。在含fs188肿瘤的皮肤中(图9C、F、I),真皮/皮下组织内仍有血管形成的证据,但是大多数可见血管位于肿瘤内部,位于深度约为600 μm的横纹肌层正下方,最大直径约50 μm(红色箭头)。
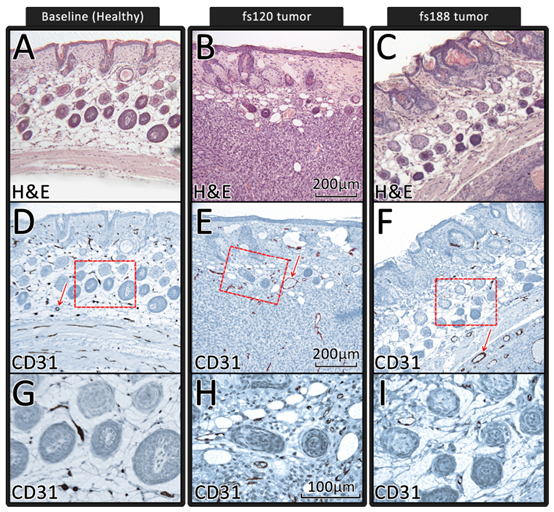
一般来说,该系统的穿透深度足以捕获fs120和fs188肿瘤内的浅层脉管系统,但在某些特定位置,轴向深度穿透仍取决于上皮层中是否存在高散射结构。图7B、D、F中可见表面散射结构(如毛囊)的带状阴影,这些阴影可能会遮挡正下方血管的血管造影信号。
04-定量血管度量
血管造影图像二值化产生血管骨架,从而定量血管参数。结果发现,fs120肿瘤(60.7 ± 4.9 μm)的平均血管直径明显高于fs188肿瘤(45.0 ± 4.0 μm),与之前使用窗室模型的活体观察研究结果一致。Vakoc等人已经证明了窗室模型成像的背景下对于大血管,多光子显微术和OCT血管造影之间具有良好相关性,但对直径小于12 μm的毛细管相关性较差。考虑到fs188肿瘤血管形态较薄,对fs188平均血管直径测量的影响可能比对fs120更大,但不同肿瘤类型之间的差异仍然显著。

图10. fs120肿瘤(n = 9)和fs188肿瘤(n = 8)间定量血管参数的变化。
fs120肿瘤每平方毫米的总血管长度(4.3 ± 1.5 mm-1)明显大于fs188(2.2 ± 0.7 mm-1),fs120肿瘤的总血管密度(31.7 ± 11.1%)也比fs188肿瘤(14.8 ± 5.0%)高,与之前研究得到的密度计算值一致。而之前的窗室模型中得到的结果与此相反,fs120肿瘤每平方毫米总血管长度较低。这很可能是不同深度或量化方法造成的。事实上由于fs188肿瘤浸润性较弱,脉管系统处于较表层皮肤中,而本所用文骨架化是在0-800 μm的大深度范围内进行的,这将直接导致检测到的整个fs188脉管系统的长度减少。但相同组织深度直接比较,fs120中深处血管又会被浅表血管的阴影所遮挡,产生不准确结果。因此本研究只考虑前100 μm的可见脉管系统,将脉管系统与组织深度分离,得出的fs120肿瘤每平方毫米血管长度(1.5 ± 0.7 mm-1)显著低于(p = 0.04)fs188肿瘤(2.2 ± 0.3 mm-1)。仍不能确认诸如总血管长度/密度之类的深度相关度量是否可靠。
不同肿瘤类型之间平均血管段长度没有显著差异,与之前的窗室模型观察结果一致。fs120组中的血管网络的平均弯曲度和分形维数(分别为1.56 ± 0.29和1.33 ± 0.17)都显著高于fs188组(分别为1.33 ± 0.13和0.98 ± 0.18)。考虑到不同肿瘤类型之间的平均血管段长度没有差异,fs120肿瘤中弯曲度较高意味着fs120血管网络的分支点比fs188肿瘤的分支点靠得更近,而不是分支点之间的血管本身更弯曲。这反映在分形维数测量中,fs188s的分形维数较低,表明血管网络更规则、更有组织。这也与之前用活体显微镜对这些肿瘤类型的观察相一致,即fs120血管通常较宽且排列非常混乱,而fs188血管规则排列且均匀狭窄。
总结
本文使用OCT系统成功地非侵入性地量化了皮下植入的表达不同血管内皮生长因子亚型的小鼠肿瘤的浅表脉管系统的形态学差异,获得的结果与先前研究中常规方法结果一致。证明使用OCT无需手术干预即可测得肿瘤血管的已知形态学差异,不但允许对肿瘤进行三维环境中的生长和观察,还可实现纵向监测。为肿瘤研究提供了新思路,也为临床治疗护理提供了非常有价值的工具。
推荐仪器




