来宝网 2025/3/14点击67次
过去20年间(2004-2024),从侵入式肌电(iEMG)到表面肌电(sEMG),从分立式电极到高密度电极,肌电信号的采集和分析技术取得了突破性进展,其应用范围从监测肌肉激活、估计肌纤维传导速度扩展到解码神经控制信息。英国帝国理工学院教授、著名电生理学家Dario Farina在2004年发表了一篇综述,讨论了表面肌电神经控制策略的应用、潜力以及局限性。当时,sEMG采集和处理几乎完全局限于提取信号的全局特征,例如幅度和功率谱,用于挖掘这些变量与生理机制相关性。尽管这些全局特征也在一些研究中被证实与神经驱动建立映射,但这些变量受到运动单位相对于电极位置的强烈影响,且在神经驱动可解释性层面存在明显局限性。在这篇综述发表的后十年间(2004-2014),出现了许多关于使用sEMG测量神经连接的研究,表面肌电分解技术也成为现实,然而这些技术所需信号质量和通道数量要求较高,仍需全面验证。如今,得益于高密度肌电采集技术,表面肌电分解已成为一种成熟且经过验证的技 术,用于在各种条件下分析运动单位和肌肉的神经驱动。这篇文章是Dario Farina教授近期关于sEMG在过去20年(2004-2024)发展和应用再次发表的综述,重点关注sEMG在提取神经控制策略方面的进展。文章分为三个主要部分:sEMG建模、sEMG处理以及sEMG在神经接口等方面的应用。

图1 Dario Farina最新综述。
sEMG建模进展
sEMG建模是理解肌电信号生成和解释的关键,特别是用于教学、信号分析和可解释性研究、信号处理、算法验证和估计不可测参数等应用。其中一个重要应用是,sEMG建模相关研究揭示了信号生成的复杂性,尤其是小运动单位对总信号幅度的贡献会随着信号强度增加而减少,这不仅由于其相对幅度降低,还因为小动作电位更容易发生幅度抵消。因此,从sEMG幅值难以用于获取神经驱动信息。另一个重要应用是串扰,即通过容积传导传播到远离肌肉激活位置处所采集的sEMG。对sEMG建模研究揭示了串扰的复杂性,例如其频域特性并不符合低通滤波的假设,进一步说明容积传导对信号传播的影响。尽管早期的模型主要基于简单的几何形状,如平面和圆柱体,这些模型虽做出了较大地简化,但在教学和基础研究中发挥了重要作用。
近年来,sEMG信号建模取得了显著进展,特别是在有限元建模(FEM)和神经网络的应用。FEM模型通过优化计算负载和简化数值解算法,使得复杂模型的计算更加高效,并为神经网络训练提供了基础。特别是基于MRI的有限元模型,能够精确反映肌肉和周围组织的真实形状和电导特性(图2)。例如,BioMime模型作为一种先进的神经网络,能够通过学习复杂的生物物理过程快速生成接近真实的sEMG信号,并在解剖学准确的容积传导中模拟运动单位动作电位的传播,包括串扰信号的影响。这些先进模型不仅能够作为实际sEMG记录的数字孪生,通过与实验数据的匹配识别关键神经肌肉属性,还能为个性化医疗和更精确的电极设计提供支持。尽管复杂模型的计算成本较高,但它们能够提供更深入的生物学和生理学理解,并有望推动sEMG技术在临床应用中的发展,例如提高运动单位数量估计(MUNE)的准确性和表面肌电技术的临床转化。
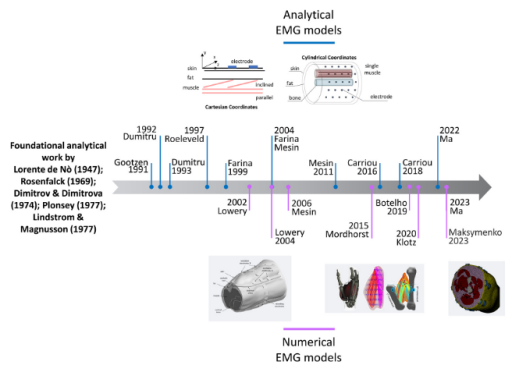
图2 sEMG的解析和数值模型示例,包括平面和圆柱体解析模型以及基于MRI的数值模型,涵盖了从1947年到2023年的多个研究。
sEMG信号处理进展
信号处理领域在过去几十年中取得了显著进展,尤其是sEMG分解技术的发展。自2014年以来,sEMG分解算法在多种复杂条件下得到了广泛验证,包括快速收缩和高同步性运动单位的诱发收缩。这些验证不仅证明了分解技术的有效性,还揭示了其在不同肌肉解剖结构中的适用性(图3)。尽管仍存在一些局限性,如对深层和小肌肉运动单位的解码困难,但sEMG分解已成为研究人类运动单位活动的有效工具。近年来,sEMG分解技术取得了显著进展,包括跨会话追踪运动单位、增加识别的运动单位数量、在动态收缩中的应用以及实时信号分解的实现。基于盲源分离算法的实时分解技术,能够在几十毫秒内完成信号分解,该方案成为神经接口(如假肢控制)的核心组成部分。随着神经网络等新技术的应用,sEMG分解的准确性和鲁棒性有望进一步提高,推动其在临床和研究中的更广泛应用。
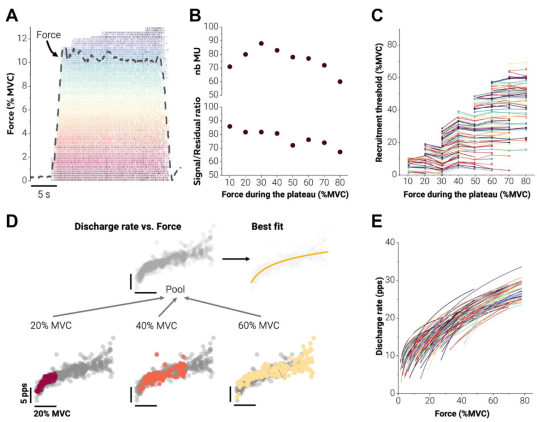
图3 通过HD-sEMG记录的胫骨前肌在不同目标力量下的运动单位放电率编码,追踪了187个运动单位在不同收缩力下的活动,并通过自然对数函数拟合了运动单位放电率与力量之间的关系,揭示了运动神经元的输入-输出特性。
人工智能(AI)技术在sEMG信号分解中的应用逐渐兴起,展现出巨大的潜力(图4)。一方面,AI增强的信号分解方法通过深度神经网络从经典源分离技术中学习,并将其应用于新数据,显著提高了对噪声的鲁棒性,这主要得益于数据增强技术,例如在训练数据集中添加实验数据的噪声版本,使神经网络对噪声的敏感性降低。这种方法不仅可能解决手动检查分解结果的繁琐问题,还为未来的临床应用提供了新的思路。另一方面,无监督神经网络也被引入sEMG分解,通过将信号映射到低维流形并施加约束来解决分解问题,无需依赖经典算法的训练,为sEMG分解带来了新的可能性。尽管AI在信号分解中的应用仍处于早期阶段,但其对sEMG信号分析的影响已经十分显著。未来,随着数据增强和个性化模型的发展,AI有望进一步提高sEMG分解的鲁棒性和准确性,推动该技术在临床和研究中的广泛应用。
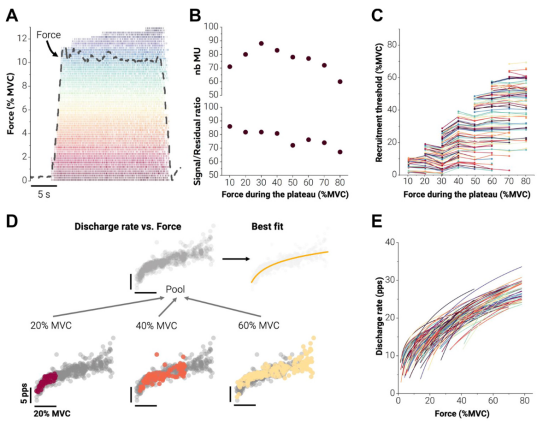
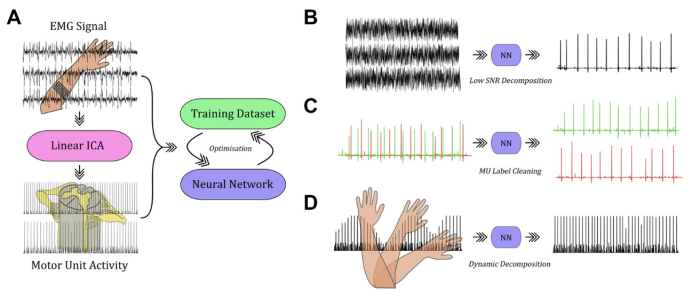
图4 基于人工智能增强的肌电分解方法,通过训练深度神经网络预测运动单位活动、识别分解中的误判,并补偿信号非平稳性,提升了肌电分解的准确性和鲁棒性。
sEMG的应用
sEMG作为研究运动单位的工具,在过去20年中取得了重要进展,实现了从全局和基础方法向非侵入性识别单个运动单位的动作电位放电时间的转变。这一进展不仅推动了基础生理学研究,还扩展了sEMG信号与其他设备的接口应用。肌电控制是其中一个重要领域,利用sEMG信号作为人机接口控制外部设备,如主动假肢。通过记录截肢者残余肌肉的sEMG信号,可以推断用户的运动意图,并将其转化为控制假肢的命令。尽管肌电控制已应用数十年,并在商业假肢中实现,但其临床转化仍面临挑战,如计算资源需求和信号鲁棒性问题。
通过分解残余的sEMG信号,研究人员能够解码脊髓损伤患者的运动神经元活动,这些活动在患者执行手部任务时是受意志控制的。因此,解码后的运动神经元活动原则上可以作为神经接口,用于提取用户的意图并控制虚拟手或辅助设备,如外骨骼手套或功能性电刺激。如图5所示,这种接口的准确性足以将运动神经元活动与预期的手部动作精确关联。尽管目前这一应用仅处于概念验证阶段,但初步结果显示出巨大的潜力。
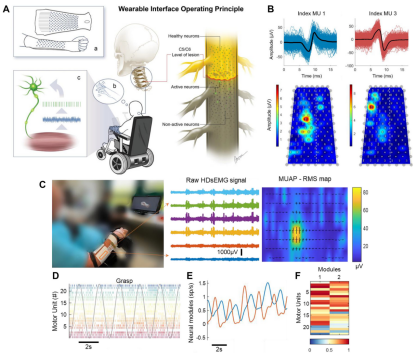
图5 通过袖套电极阵列记录脊髓损伤患者前臂肌肉的sEMG信号,尽管患者无可见运动,但仍能检测到肌电信号并分解出单个运动单位活动,揭示了运动神经元放电与手部任务意图的关联。
通过在线估计单个运动单位的放电时间,研究人员开发了基于肌肉神经驱动的高级生物反馈系统。由于接收共同输入的运动神经元群体具有线性输出特性,可以从sEMG解码运动神经元的输出(即对肌肉神经驱动的估计),进一步估计相应的共同输入信号。这些生物反馈系统已用于证明中枢神经系统无法独立控制单个运动神经元,而是将共同突触输入分配给一组运动神经元。此外,皮质振荡活动(如β波和γ波)也通过共同投射传递到运动神经元群体,影响肌肉力的产生。下图展示了一个模拟示例(图6),表明可以从运动神经元群体的输出中提取不同频率的输入信号。尽管与振荡活动的接口在治疗性生物反馈和人类增强方面具有潜在应用,但目前的结果仍处于初步阶段,存在诸多挑战。令人欣喜的是,sEMG在神经接口中的应用在过去十年中引起了广泛关注,其中不乏知名科技公司也积极参与其中。
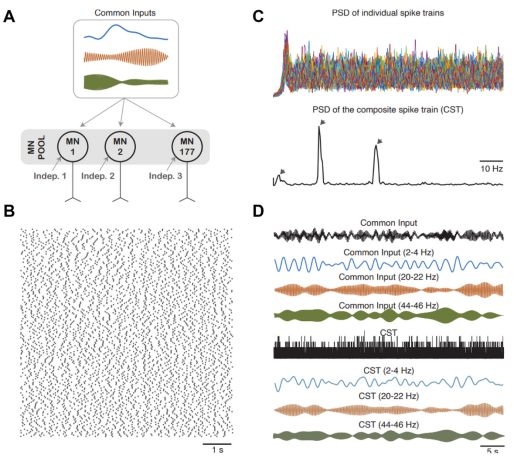
图6 通过模拟177个运动神经元接收共同输入和独立输入的解码过程,揭示了运动神经元群体对振荡性输入的线性响应,并通过滤波重建了输入信号的频率成分。
总结与展望
在过去20年中,sEMG在神经控制策略的研究中取得了显著进展,但仍存在一些挑战。如sEMG在临床神经生理学中的应用尚未标准化,传统的侵入性EMG(如,同心针电极)仍然是诊断神经肌肉疾病的主要方法。sEMG信号的滤波效应使得一些临床相关特征难以检测,因此将其转化为常规临床评估和监测工具仍是一个关键挑战。此外,尽管sEMG在运动医学、神经康复和职业医学等领域有广泛应用,但其临床转化和采用仍然有限,部分原因是技术复杂性和缺乏广泛的教育与推广。未来,随着技术的进一步发展和标准化,sEMG将成为研究神经肌肉控制不可或缺的工具,并在临床医学中实现更广泛的应用,这一技术的潜力无疑将在未来的科研和临床实践中得到进一步挖掘。
参考文献
D. Farina, R. Merletti, and R. M. Enoka, “The extraction of neural strategies from the surface EMG: 2004–2024,” J. Appl. Physiol., vol. 138, no. 1, pp. 121–135, Jan. 2025, doi: 10.1152/japplphysiol.00453.2024.
关于维拓启创
维拓启创(北京)信息技术有限公司成立于2006年,是一家专注于脑科学、康复工程、人因工程、心理学、体育科学等领域的科研解决方案供应商。公司与国内外多所大学、研究机构、企业长期保持合作关系,致力于将优质的产品、先进的技术和服务带给各个领域的科研工作者,为用户提供有竞争力的方案和服务,协助用户的科研工作,持续提升使用体验。
相关产品




